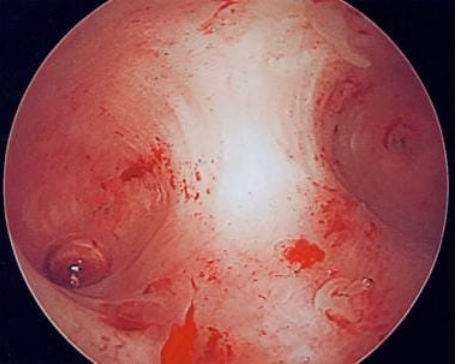
宫腔镜手术是一种微创妇科手术,其中将内窥镜光学镜片通过子宫颈插入子宫内膜腔,以直接治疗各种类型的宫内病变。
适应症
(1)异常子宫或大量月经出血;
(2)宫腔镜检查经常用于评估异常子宫出血 (AUB) 或大量月经出血 (HMB),特别是在先前研究(即子宫内膜活检和盆腔超声检查,有或没有向子宫内膜腔内注入生理盐水)不明确或证明病理。
在解剖异常导致 AUB 的情况下,手术宫腔镜允许同时诊断和治疗。 对于不希望将来生育的特发性月经过多的女性,可以在宫腔镜手术(即滚球、激光和水热消融)期间或宫腔镜手术(即,NovaSure、Thermachoice 和冷冻消融术)之后进行伴随的子宫内膜消融。
粘膜下肌瘤
如果认为黏膜下肌瘤是 AUB 或不孕的病因,则需要宫腔镜切除黏膜下肌瘤。 欧洲妇科内镜学会将粘膜下肌瘤分为 0、1 或 2 型。0 型粘膜下肌瘤完全位于子宫内膜腔内,而 1 型肌瘤的壁内成分小于纤维瘤直径的 50%。2 型粘膜下肌瘤的壁内成分占直径的 50% 以上,通常需要通过剖腹手术或腹腔镜手术切除。
宫腔镜子宫肌瘤切除术对于 0 型和 1 型粘膜下肌瘤疗效最佳。然而,在看似完全切除之后,肌瘤的残余壁内成分可能会进入子宫内膜腔。具有大量壁内成分的大型黏膜下肌瘤可能需要多次单独手术才能切除整个肌瘤。15-20% 的宫腔镜子宫肌瘤切除术需要随后的手术来治疗持续的症状或残留的肿瘤。 在进行手术之前,建议使用诊断性宫腔镜检查、盐水输注宫腔声波图 (SIS) 或盆腔 MRI 对患者的解剖结构进行完整表征。
子宫息肉
子宫内膜息肉可引起 AUB,也可能与不孕症有关。有子宫内膜癌危险因素的子宫内膜息肉患者有恶变倾向。因此,需要通过诊断性宫腔镜检查或超声检查发现息肉切除。
子宫中隔
子宫中隔是受中线融合后苗勒管不完全内侧退化的胚胎学影响,可能通过子宫输卵管造影 (HSG)、SIS 或盆腔 MRI 或在不孕或复发性流产的检查过程中偶然发现。子宫隔膜被认为是 RPL 的主要病因,切除术显著提高了活产率。 子宫中隔切除术是通过剖腹手术和子宫切开术切口进行的,发病率很高。剖腹手术已在很大程度上被宫腔镜检查取代,作为对子宫中隔的一种不太病态的干预。
溶解粘连
宫内粘连 (IUA)、粘连或 Asherman 综合征是产科或非产科子宫器械或泌尿生殖道感染的结果。子宫粘连可导致 AUB、不孕症或 RPL,可通过 HSG 或 SIS 进行诊断。 宫腔镜切除术是有症状的宫腔粘连的标准治疗方法。在由子宫粘连引起的不孕或 RPL 的情况下,病变的密度和子宫内膜闭塞的数量直接影响粘连松解后的后续妊娠和活产率。
输卵管口置管
近端输卵管闭塞通常在不孕症检查期间在 HSG 上发现,病因多种多样,包括盆腔炎(PID)、输卵管痉挛、子宫内膜异位症、结节性输卵管炎、息肉和粘液堵塞或输卵管碎片。 宫腔镜近端管插管可用于打开阻塞的管,通常与腹腔镜检查同时进行,以便评估远端输卵管疾病的可能性,并可以通过chromopertubation 确认输卵管通畅。
取出异物
保留的宫内节育器 (IUD)是最常见的宫腔异物。然而,另一种罕见的病因是终止妊娠后残留的胎儿骨骼。偶尔会遇到无法定位宫内节育器的情况,这通常是由于放置后串被剪得太短造成的。此外,宫内节育器在放置后可能会移动或在插入过程中或长时间使用后嵌入子宫肌层壁中。
在尝试取回装置之前,获取超声图像,并在需要时进行其他放射学研究,以定位宫内节育器。各种程序和工具可以帮助临床医生移除缺少绳子的宫内节育器,包括挂钩装置和抽吸刮匙、抓握工具和取线装置。取回宫内节育器后,检查装置以确保已将其全部取出。
宫腔镜也可用于定位、抓取和取出子宫腔内的异物。因为宫内节育器也可能穿孔了子宫壁,所以在宫腔镜检查之前应该进行腹部成像以帮助定位。使用并发腹腔镜检查可能有助于移除迁移、穿孔或深度嵌入的设备。
消毒
现在可以使用宫腔镜替代腹腔镜或小开腹手术灭菌技术,这些技术可以在门诊环境中进行,只需少量麻醉或无需麻醉。
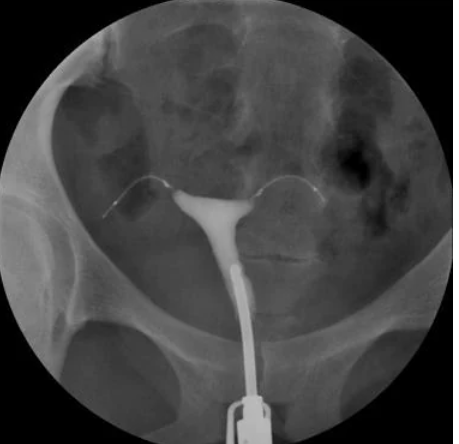
双侧输卵管阻塞
Essure (Conceptus) 是一种程序,其中由围绕聚对苯二甲酸乙二醇酯 (PET) 纤维的镍钛 (镍钛诺) 组成的微插入线圈在宫腔镜下放入近端输卵管。线圈将装置固定在适当的位置,而 PET 纤维刺激组织的纤维化向内生长,从而导致输卵管腔永久闭塞。
禁忌症
很少注意到宫腔镜手术的禁忌症。这些包括怀孕、宫颈炎活动性盆腔感染、已知的宫颈癌或子宫内膜癌以及外科医生经验不足。血管内容量扩张可能加剧的合并症是相对禁忌症。 此外,已知对镍过敏的患者不应进行 Essure 绝育,并且对放射造影剂过敏的患者不适合进行宫腔镜绝育手术。
子宫肌瘤切除术
可以使用电切镜或双极子宫镜切除黏膜下肌瘤。两种手术宫腔镜都允许电灼切除肌瘤。如前所述,电切镜使用单极烧灼和非电解质扩张介质,而双极电切镜使用电解质介质。使用任一宫腔镜,通过手术端口放置一个 90° 环形电极。
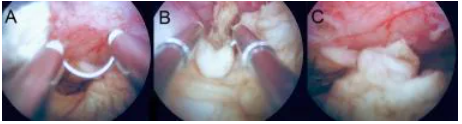
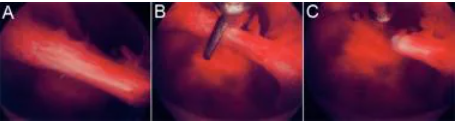
宫腔镜子宫肌瘤切除术
(A):90° 环形电极从外护套延伸。
(B):电极已延伸到肌瘤之外,并通过弹簧机构缩回到外鞘中。
(C):肌瘤碎片在子宫内膜腔内自由漂浮。
然后将环推进通过肌瘤;应用 80 至 100 瓦的连续波(切割)电烙术,然后将环缩回到手术鞘中。
为了最大限度地减少热损伤和子宫穿孔的风险,应仅在回缩环时施加电能。随着电极向后缩回,一条平滑肌瘤被切除并漂浮在子宫内膜腔中。这种技术被重复多次,直到肌瘤被完全去除。产生的纤维瘤组织碎片可能开始阻碍可视化。如果发生这种情况,将宫腔镜从宫腔中取出,用息肉钳盲目地从宫腔中取出肌瘤碎片并送去进行组织病理学检查。或者,可以使用排屑系统。反复取出和插入宫腔镜会增加子宫穿孔、空气栓塞、体液不足计算错误或血管内渗入的风险,应避免。
当肌瘤基底与邻近的子宫肌层齐平时切除,因为超过这一点的切除会增加子宫穿孔的机会。或者,外科医生可以停止切除并允许周围的子宫肌层收缩并将剩余的肌瘤组织输送到腔内。前列腺素 F 2α卡前列素给药已被证明有助于将残余肿瘤输送到子宫腔中。
具有明显壁内成分的粘膜下肌瘤是在单一手术中完成切除的障碍。在这些情况下,“冷循环”技术被认为是一种有益的方法。在这种技术中,通过在不施加电流的情况下用电切镜环推拉将肌瘤囊与周围的子宫肌层分离。
肌瘤的全部摘除术。该过程包括在子宫内膜上的肌瘤上创建一个椭圆形切口,然后结合钝器和电灼解剖。
宫腔镜粉碎器也可用于进行子宫肌瘤切除术。一旦宫腔镜插入子宫腔,手机就会通过独特设计的宫腔镜手术通道放置,并用于粉碎注意到的肌瘤。手柄远端的窗口应靠近肌瘤的粗糙或不规则边缘。见下图。
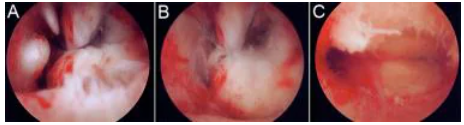
子宫肌瘤切除术和息肉切除术
(A):注意到多个小的 0 型和 1 型粘膜下肌瘤,以及子宫内膜息肉。
(B):当使用往复式手机粉碎肌瘤时,肌瘤被输送到子宫内膜腔中。
(C):手术后子宫内膜腔没有病理变化。
用脚踏板启动切割动作,通过吸力将肌瘤吸入。见下图。
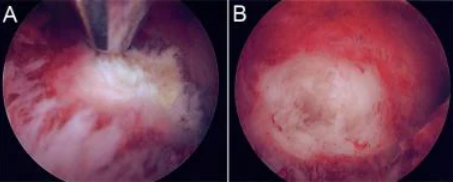
(A):肌瘤通过窗口被吸入往复式手机的刀片。
(B):平滑肌瘤的腔内部分已被粉碎至邻近子宫肌层的水平。残留的壁内肿瘤仍然存在。
息肉切除术
宫腔镜息肉切除术可以使用几种不同的技术来完成。第一种选择是将标准硬质宫腔镜放入子宫腔,并使用通过手术端口插入的抓钳去除注意到的息肉。夹钳应指向息肉底部,并在通过宫腔镜取出夹钳时保持夹钳压力。可能需要多次尝试才能完全去除息肉。这种方法通常可以很好地耐受,只需少量或仅局部麻醉。与上述的子宫肌瘤切除术技术相似,带有 90º 环的单极或双极电切镜可用于切除更大或更多的子宫内膜息肉。
另一种技术涉及使用宫腔镜粉碎装置;当在腔内观察到多个息肉时,对于大多数宫腔镜息肉切除术,分碎术快速有效,并且可以收集标本,以便进行病理检查。一旦手持件插入手术通道,器械的窗口就被放置在息肉最远端附近,切割动作通过脚踏板进行。当吸力将息肉通过窗口吸入粉碎刀片时,手持件保持静止。见下图。
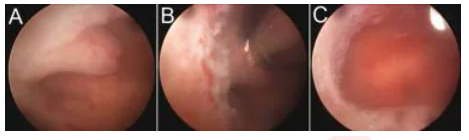
息肉切除术
(A):子宫内膜息肉。
(B):息肉的远端被抽吸到旋转手机的窗口中。
(C):手术后子宫内膜腔没有病理变化。
扫过子宫内膜表面可能有助于去除多个息肉和蓬松的子宫内膜。
成形术
子宫中隔切除术(也称为子宫内膜成形术或中隔成形术)可以使用内窥镜剪刀、电烙术、钕:钇铝石榴石 (YAG) 激光或宫腔镜粉碎器进行,但最好使用标准的硬质宫腔镜进行和内窥镜剪。插入内窥镜并识别隔膜后,通过手术通道放置宫腔镜剪。见下图。
子宫中隔
输卵管口的双侧可视化至关重要,因为口是整个切除过程中的地标。
外科医生可以根据需要朝每个开口头侧和侧向工作。在前倾子宫中进行切除后,在后倾子宫中进行前切除的趋势已被识别。在每次用剪刀切开之前,应观察开口,外科医生应确认定位在正确的平面上。子宫肌层血管非常丰富,如果切开会出血。出血表明切除线太靠前或靠后,或者已经到达子宫底肌层。
宫腔镜手术切除的替代方法包括在 70 至 100 瓦的混合(凝固)设置下使用单极或双极烧灼。0°环形电极可通过电切镜或双极手术宫腔镜的手术通道插入,并可用于以与上述类似的方式分割隔膜。
插入腹膜腔的内窥镜透镜可用于可视化来自宫腔镜的透照,表明子宫肌层变薄。当外科医生使用电灼或激光分割隔膜时,建议进行腹腔镜检查,但如果使用剪刀或粉碎器,则可以省略此步骤。经腹超声检查也可用于指导切除子宫中隔。
为了改善子宫腔的可视化,通过 Foley 导管在膀胱中填充 300-500 mL 无菌生理盐水,然后夹住导管。然后将经腹超声探头放置在下腹部,外科医生通过宫腔镜和超声成像的直接可视化组合来指导切除。在麻醉逆转之前排空膀胱。
取出宫腔镜后,使用子宫敷料钳放置三角形气球子宫支架,并用1-5毫升生理盐水或水充气。如果外科医生选择使用球囊或 Foley 导管,患者应接受雌激素治疗和抗生素预防(强力霉素 100 毫克,每天两次)。 [ 31 ] 使用雌二醇贴剂(0.1 毫克/天)或口服片剂,直到球囊停止使用。球囊放置后 10-14 天应在门诊放气并取出。
溶解粘连
使用标准刚性手术宫腔镜切开子宫粘连。将内窥镜放入子宫内膜腔后,宫腔镜剪通过手术通道推进并用于分离任何明显的粘连。见下图。
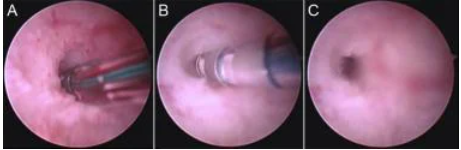
宫腔粘连横切
(A):跨越子宫内膜腔的宫腔粘连。
(B 和 C):宫腔镜剪通过刚性宫腔镜的手术通道插入并用于横切粘连。
粘连溶解应从位于最中心的粘连开始,然后进行到位于空腔外围的粘连。也可以使用 YAG 激光或 0° 单极或双极电烙环通过电切镜或双极手术宫腔镜插入子宫粘连进行横切。
致密粘连可能需要使用电切镜或双极电烙环。在涉及广泛或致密粘连溶解并明显闭塞子宫内膜腔的情况下,同时进行腹腔镜切除术以降低穿孔风险。与宫腔镜中隔成形术一样,在广泛切除后子宫内膜破裂的患者可能会受益于术后放置宫内球囊或 Foley 导管和如上所述的雌二醇治疗。
输卵管插管
导管由一根由内套管和外套管包围的导丝组成。放置硬性宫腔镜后,将插管通过内窥镜的手术通道放置到子宫腔中。
外套管稍微弯曲以方便放置,位于开口之一附近。然后将内套管插入近端导管约 2 cm,绕过或治疗闭塞的病因,并移除导丝。然后通过导管注入稀释的靛蓝胭脂红或亚甲蓝溶液,通过同步腹腔镜检查可以观察到来自远端管的染料溢出。然后从口中取出两个套管,并在对侧重复该过程。Novy 导管是灵活的,但可能会导致输卵管穿孔。 因为导管的直径如此小,穿孔通常是止血的并且不需要修复。
取出异物
保留的宫内节育器(IUD)是最常见的宫腔异物。手术宫腔镜后,通过手术通道插入抓钳,用于抓握宫内节育器的绳子或柄。然后将整个宫腔镜装置连同异物一起从腔中缓慢取出。在某些情况下,宫内节育器可能嵌入子宫内膜或子宫肌层中,需要在取出前进行一定程度的解剖。在这些情况下,同时进行腹腔镜检查可能有助于避免子宫穿孔。
消毒
带有 5 French 手术口的标准硬质宫腔镜可用于宫腔镜消毒。插入宫腔镜后,应首先确定双侧开口,因为这是成功完成手术所必需的。
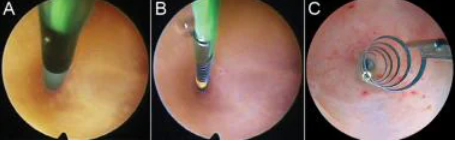
微型插入物的输送可以通过刚性宫腔镜的手术通道进行。最外面的输送导管的尖端首先插入子宫内膜腔,然后插入输卵管口至预先标记的深度。当输送导管缩回到装置手柄中时,释放导管或内部导管就会显露出来。当内部释放导管缩回时,微型插入件展开并固定在输卵管壁上。然后分离并移除导丝。然后在对侧执行相同的程序。手术后应在子宫内膜腔中看到 4 到 8 个完整的线圈。
(A):将输送导管插入口部至黑色带的水平并收回。
(B):然后将释放导管收回,使微型插入物展开并固定在输卵管壁上。
(C):导丝被分离并移除。在子宫内膜腔中可以看到五个完整的线圈。
(A):将输送导管插入口部至黑色带的水平。
(B) 在提供射频能量后,硅胶插入物被部署,导管被移除。
(C):放置插入物后的输卵管口。
并发症
宫腔镜手术是一种安全的手术,会导致 0.95-3% 的病例出现并发症。最常见的并发症包括出血、子宫穿孔和宫颈裂伤;另一种罕见的并发症是液体吸收过多,伴有或不伴有低钠血症。
子宫穿孔
子宫穿孔是宫腔镜手术最常见的并发症之一,发生率为0.7-3%。患者应该意识到可能需要同时进行腹腔镜检查。子宫穿孔最常发生在粘连松解术,其次是子宫肌瘤切除术和隔膜切除术,但也可能发生在宫腔镜插入过程中。穿孔通常通过直视来诊断,但在不明原因的液体缺乏迅速增加、不受控制的出血和血流动力学不稳定的情况下,也应怀疑穿孔。子宫探查器、宫颈扩张器、宫腔镜或其他钝器引起的子宫底止血穿孔可以保守治疗。
麻醉后监护室的观察应包括监测生命体征、尿量,在某些情况下还应监测血细胞比容。由于有可能损伤盆腔脏器或脉管系统,通过后子宫或外侧子宫或尖锐或电灼器械穿孔应立即进行腹腔镜检查。如果发现前部穿孔,应进行膀胱镜检查以评估膀胱损伤。
液体过载和电解质失衡
液体吸收过多的发生率为 0.2-0.76%,是宫腔镜手术潜在的严重并发症。子宫肌瘤切除术、子宫中隔切除术、粘连的广泛溶解和延长的手术时间会增加临床上显着的体液超负荷和低钠血症的风险,尤其是在使用低渗膨胀介质时。
如果大量吸收,不含电解质的膨胀介质会导致快速而严重的低钠血症。出于这个原因,应仔细管理液体不足,并将宫内压力保持在平均动脉压以下。一旦液体不足达到 750 mL,外科医生应计划完成手术。当非电解质流体的不足达到 1500 mL 和等渗流体的不足达到 2500 mL 时,操作终止。
血清钠水平的突然变化(通常为 135-145 mEq/L)可导致精神状态改变并进展为癫痫发作、昏迷,甚至死亡。如果术中或术后钠水平低于 125 mEq/L,则应将患者转至急症或重症监护室。可按1~1.5 mEq/L/h的速度静脉给予3%氯化钠,并应使用速尿以达到适当的利尿量。在等渗液体渗入过多的情况下,会发生液体超负荷导致肺水肿。由于不降低静脉输液速度以补偿膨胀介质的宫腔镜吸收,这个问题可能会更加复杂。此外,由于液体的渗透特性,摄入相对少量的葡聚糖 70会导致血管内容量显着膨胀。
出血
宫腔镜检查期间或之后可能会出现出血。外科医生应首先确保注意到的出血不是子宫穿孔的结果。轻度出血通常是自限性的,通常不需要干预。如果发生快速出血,可以使用电灼术来凝固小血管。如果这些保守方法无法控制大量出血或较大血管出血,可以将 Foley 导管或宫内球囊插入腔内并充气以压塞出血。Foley 导管可以连接到收集袋以监测失血量。
罕见并发症
根据所进行手术的程度,宫腔镜手术可能会出现额外的、罕见的并发症。子宫中隔切除术和子宫肌瘤切除术与术后宫腔粘连形成和后续妊娠中的子宫破裂有关。宫颈内的假通道可能是由于宫腔镜插入过度或方向错误或宫颈扩张不足造成的。此外,握柄放置不当或用力操作可能会导致宫颈撕裂;使用延迟可吸收的多丝缝合线可以轻松修复子宫颈的出血撕裂伤。虽然罕见,但如有必要,使用广谱抗生素治疗术后子宫内膜炎。气体栓塞极为罕见。
术后注意事项
无并发症的宫腔镜手术后的术后病程通常不显著。由于大多数宫腔镜手术是在门诊进行的,因此患者可以在 PACU 短暂停留后的同一天回家。患者能够在耐受的情况下恢复正常饮食。对于接受广泛切除术的患者,手术后 1-2 周出现痉挛或阴道出血是正常的。对于希望在息肉切除术后立即生育的女性,可以在接下来的月经周期尝试怀孕。
如果进行了子宫内膜成形术或粘连松解术,或者如果子宫肌瘤切除术导致去除了具有相当大壁内成分的肌瘤,则应推迟 3 个月妊娠,并考虑采取避孕措施。隔膜成形术(88%)或粘连松解术(76%)后新的宫腔粘连形成率高于子宫肌瘤切除术(40%)或息肉切除术(0%)。 阴道分娩是宫腔镜下 0 型或 1 型肌瘤切除术后可接受的分娩方式。
患者通常会在手术后 2-4 周进行术后随访。在某些情况下,可能需要重复进行解剖学检查(即盐水输注宫腔声波图 [SIS] 或诊断性宫腔镜检查),以确保不形成粘连或完全切除肌瘤或隔膜。