
对于激素受体 (HR) 阳性、HER2 阴性的乳腺癌患者,当无需手术即可做出治疗时,可以使用新辅助化疗。在 HR 阳性、HER2 阴性疾病的绝经后患者中,激素治疗可用于减期疾病。淋巴结阳性或高危淋巴结阴性、HER2 阳性患者应接受新辅助治疗并结合抗 HER2 阳性治疗。本文概述了基于临床表现、患者特征和乳腺癌亚型对制定有关全身新辅助治疗的使用建议。
哪些乳腺癌患者适合进行新辅助全身治疗?

(1)新辅助化疗是炎症性乳腺癌(IBC)患者或无法切除或局部晚期的患者的首选治疗方法,这些患者可以通过新辅助治疗进行治疗。
(2)肿瘤组织学、分级、分期和雌激素、孕激素和 HER2 表达应常规用于指导是否进行新辅助治疗的临床决策。没有足够的证据支持使用其他免疫化学标志物、形态学标志物【例如,肿瘤浸润淋巴细胞(TIL)】或基因组图谱来指导是否进行新辅助化疗的临床决策。

(3)高危 HER2 阳性或 TNBC 患者提供新辅助全身治疗,其中残留病灶的发现将指导与辅助治疗相关的建议。
(4)提供新辅助全身治疗以减少手术范围(BCS 和腋窝淋巴结清扫术)。可以提供化疗加或不加靶向治疗,或内分泌治疗(如果HR阳性)。
(5)对于希望延迟手术的患者(例如,进行手术治疗所需的基因检测,以便有时间考虑选择)或不可避免的患者,可以提供新辅助全身治疗。
不能手术的局部晚期乳腺癌(LABC)或 IBC 患者。没有现代大型随机临床试验专门针对 IBC 或 LABC 患者,这些患者通常被排除在辅助和新辅助治疗试验之外。这些患者的新辅助治疗建议代表了专家小组基于Ⅱ期试验数据、较早发表的非随机数据、专家共识意见和临床经验的最佳临床意见。
新辅助全身治疗为 LABC 或 IBC 患者提供了一系列潜在优势,包括原发肿瘤降期以实现可操作性;更迅速地治疗亚临床远处微转移;增强体内评估肿瘤对特定全身性药物反应的能力。
使用免疫组织化学标志物或基因组图谱来指导新辅助治疗的临床决策。没有随机试验直接解决使用基因组谱来指导新辅助治疗决策的问题。专家组反对使用非常规免疫组织化学标志物、形态学标志物(例如 TIL)或基因组图谱来指导新辅助化疗的临床决策的建议代表了其基于目前有限的前瞻性数据的最佳临床意见。
Onco型DX 复发评分和 MammaPrint 均已显示可预测辅助化疗的益处,回顾性研究报告称,高风险 Onco型DX 复发评分可能与较高的 pCR 率相关。然而,没有前瞻性试验评估基因组标志物的临床效用,以确定患者是否应该在手术前接受全身化疗或选择化疗方案。雌激素、孕激素和 HER2 表达在实践中常规用于指导靶向治疗的使用。其他免疫化学标记、形态学标记和基因组谱标记已用于研究,但没有足够的证据支持它们用于指导新辅助治疗临床决策。
在高危 HER2 阳性或 TNBC 患者中使用新辅助全身治疗。系统评价确定了两项研究,支持在高危 HER2 阳性或 TNBC 患者中使用新辅助全身治疗,在这些患者中发现残留疾病将促使辅助治疗发生变化。卡培他滨治疗残留癌辅助治疗 (CREATE-X)开放标签Ⅲ期试验,评估辅助化疗对 HER2 阴性原发性乳腺癌患者的安全性和有效性,这些患者在接受含有紫杉烷、蒽环类或两者的新辅助化疗后仍有浸润性疾病。CREATE-X 随机分配 910 名患者接受标准的术后辅助治疗,使用或不使用卡培他滨。分析显示,卡培他滨辅助治疗可延长 DFS 和 OS。在安全性分析中,卡培他滨组观察到的最常见的不良事件是手足综合征;这发生在 443 名患者中的 325 名(73.4%)。在三阴性患者亚组中(约占研究患者的 30%),接受卡培他滨治疗的患者 DFS 率为 69.8%,而对照组为 56.1%(风险比 [HR],0.58;95% CI,0.39到 0.87);OS 率为 78。8% 与 70.3%(HR,0.52;95% CI,0.30 至 0.90)。在 HR 阳性乳腺癌患者的亚组中,DFS 和 OS 的数值改善不符合统计显着性。卡培他滨组的 DFS 率为 76.4%,对照组为 73.4%(复发、继发、癌症或死亡的 HR,0.81;95% CI,0.55 至 1.17),OS 率分别为 93.4% 和 90%,分别(死亡 HR,0.73;95% CI,0.38 至 1.40)。
一项Ⅲ期临床试验比较了辅助曲妥珠单抗 (T-DM1) 与曲妥珠单抗在 I 至 III 期、HER2 阳性乳腺癌患者中进行的比较——靶向治疗。患者被随机分配接受术后 T-DM1(n=743),剂量为 3.6 mg/kg 体重,或曲妥珠单抗(n=743),剂量为 6 mg/kg,每 3 周静脉注射一次,共 14 个周期(42 周)。大多数患者 (80%)在新辅助治疗中接受曲妥珠单抗作为其唯一的 HER2 靶向治疗;大约 18% 的患者接受了曲妥珠单抗和帕妥珠单抗的双重新辅助 HER2 靶向治疗。接受辅助 T-DM1 治疗的患者中有 91 名(12.2%) 和接受曲妥珠单抗治疗的 165 名(22.2%)患者发生了侵袭性疾病或死亡。T-DM1 组的 3 年估计侵入性 DFS 显着高于曲妥珠单抗组(88.3%对77%;HR,0.50;95% CI,0.39 至 0.64;P<0.001)。同样,接受 T-DM1 治疗的患者发生远处复发的风险低于接受曲妥珠单抗治疗的患者(HR,0.60;95% CI,0.45 至 0.79)。190 名(25.7%)接受 T-DM1 的患者和 111 名(15.4%)接受曲妥珠单抗的患者发生了 3 级或更高级别的不良事件,包括血小板减少症 (5.7% vs 0.3%) 和周围感觉神经病变(1.4% vs 0%)。T-DM1 组 94 名患者(12.7%)和曲妥珠单抗组 58 名患者(8.1%)发生严重不良事件。导致 T-DM1 停用的不良事件包括血小板减少症、肝功能检查异常升高和周围感觉神经病变。无法完成 T-DM1 的患者接受曲妥珠单抗以完成一年的 HER2 靶向治疗。
CREATE-X 和 KATHERINE 试验证实,在 TNBC 或 HER2 阳性疾病患者中,新辅助治疗后残留病灶的存在与否会改变辅助治疗的治疗建议。因此,新辅助治疗是除小的、淋巴结阴性、TNBC 或 HER2 阳性肿瘤以外的所有肿瘤的治疗选择。
很少有研究涉及使用新辅助治疗来减少腋窝手术。数据表明,在淋巴结转移患者中,由于新辅助化疗而降期可能允许对腋窝进行较小范围的手术,从而减少手术并发症,如淋巴水肿和感觉迟钝。
新辅助治疗减少局部治疗。对新辅助治疗的反应可导致肿瘤降期,因此可提高肿瘤的可切除性、增强美容效果并减少术后并发症。与新辅助化疗相关的局部治疗范围减少的证据来自几项大规模随机试验,这些试验比较了早期乳腺癌患者的新辅助化疗和辅助化疗。与辅助化疗相比,所有报告都报告了新辅助治疗的 BCS 发生率增加。一些III期新辅助研究,包括CALGB 40601,的CALGB 40603,和亮度,包括事先规定的次要分析,以评估患者是否视为不是候选人在基线BCS能够被转换为BCS。在这些试验中,从不符合 BCS 到符合 BCS 的转化率在 43% 到 53% 之间。

对于可切除的肿瘤,采用适当辅助方案的新辅助全身治疗可提高保乳率,并可能减少腋窝淋巴结清扫术的需求。在 HR 阳性、HER2 阴性乳腺癌中,新辅助内分泌治疗与化疗具有相似的临床反应率,是一个合理的选择。然而,对于这种肿瘤亚型,乳房或腋窝淋巴结中的肿瘤根除很少见。
手术延迟的新辅助治疗。没有随机试验直接解决使用新辅助治疗作为延迟手术的桥梁。当首选或需要延迟手术时,可以使用新辅助治疗的建议代表了专家小组基于乳腺癌管理个人经验的最佳临床意见。
在资源有限的环境中以及在 2020 年 COVID-19 大流行等公共卫生危机期间,获得医疗资源(包括手术)的机会可能有限。在这些情况下,新辅助治疗既可用于控制局部疾病,又可在进行手术之前防止疾病的远处扩散。
此外,在临床情况下,虽然不是绝对必要,但可能更喜欢延迟手术。例如,如果一名有明确化疗指征的患者怀疑有BRCA1或BRCA2突变,并且正在考虑双侧乳房切除术,那么推迟手术可能是合理的,直到获得基因检测结果或直到可以讨论重建方案。在这种情况下,由于新辅助治疗和辅助治疗已被证明在长期结果方面是等效的,因此可以考虑新辅助治疗。
接受新辅助化疗的患者应如何预测效果?

(1)定期通过临床检查监测接受新辅助治疗的患者的反应。乳房成像可用于确认临床怀疑进展和手术计划。使用影像学时,应在随访时使用在基线时最能提供信息的方式——乳房 X 光检查、超声或磁共振成像。
(2)不应使用基于血液和组织的生物标志物来监测接受新辅助治疗的患者。
(3)pCR,定义为乳房和淋巴结无浸润性疾病,应用于衡量反应以指导临床决策。
没有随机试验的数据告知治疗期间监测反应的最佳方法。监测临床、放射学和病理学反应的频率和特征以及进展性疾病 (PD) 管理的建议反映了专家小组基于乳腺癌管理个人经验的最佳临床意见。

对于新辅助化疗后倾向于 BCS 的患者,应充分考虑在基线和化疗完成时进行影像学检查,以获得最佳手术计划。然而,由于 PD 的罕见性质,没有证据支持常规成像对进展的益处。如果临床上怀疑 PD,建议进行额外的影像检查以进行确认。应使用与基线评估相同的方式进行成像;研究表明,MRI 提供了最准确的疾病程度客观测量。如果有临床进展的证据,则应就转换治疗或进行局部区域干预做出多学科决定。
没有关于使用血液标志物(例如 CA27-29 和 CA15-3)监测治疗反应的数据,不推荐在新辅助治疗中使用这些标志物。几项研究评估了早期生物标志物(例如 Ki67)减少与乳腺癌预后改善之间的关联;然而,这些方法用于研究目的并证明对新治疗方法的评估是合理的,并不旨在指导常规临床治疗。
大多数新辅助研究使用 pCR 作为主要终点。然而,关于残留的非侵袭性疾病是否包括在 pCR 的定义中,存在很大差异。在 KATHERINE 和 CREATE-X 研究中,pCR 被定义为没有残留的侵袭性疾病。研究还评估和验证了残余癌症负担和 yP 美国癌症联合委员会(AJCC)分期预后因素的使用,这些因素与长期乳腺癌结果相关。随机临床试验中很少有证据表明如何定义和管理新辅助治疗的进展,因为试验没有一致的方法。新辅助治疗期间的进展很少见,也没有得到很好的研究;在最大的报告系列中,只有 3% 的患者确诊为 PD,超过一半的进展患者在新辅助治疗的前两个周期内表现出 PD。然而,新辅助化疗期间的进展与显着更差的无进展生存期和 OS 相关,强调了治疗期间临床监测的重要性。
虽然还没有比较不同检查肿瘤床方法的临床试验,但有大量数据表明 pCR 的发现(无论定义为没有浸润性疾病或乳房和淋巴管没有浸润性和非浸润性疾病)节点与良好的预后相关。重要的是,pCR 对于确定 TNBC 和 HER2 阳性乳腺癌是否需要额外辅助治疗至关重要。新辅助全身治疗后进行手术时,应进行细致的临床、影像学和病理相关检查,确保彻底检查瘤床有无残留病灶,并在病理报告中注明乳腺和腋窝的病变范围,使用 AJCC 分期。
对于 TNBC 患者,推荐哪些新辅助全身治疗方案?

(1)临床淋巴结阳性和/或至少为 T1c 疾病的 TNBC 患者应在新辅助治疗中接受含蒽环类和紫杉类的方案。
(2)cT1a 或 cT1bN0 TNBC 患者不应常规接受临床试验之外的新辅助治疗。
(3)卡铂可作为 TNBC 患者新辅助治疗方案的一部分提供,以增加 pCR 的可能性。提供卡铂的决定应考虑潜在益处和危害的平衡。
(4)没有足够的证据推荐在早期 TNBC 患者的新辅助化疗中常规加入免疫检查点抑制剂。
TNBC 患者的新辅助化疗。关于 TNBC 患者最佳新辅助化疗方案的 III 期随机临床试验没有直接证据。然而,基于关键随机临床试验和个体患者数据荟萃分析存在广泛共识,即适合分阶段辅助治疗的化疗方案也适用于新辅助治疗。在此基础上,专家组建议为临床淋巴结阳性和/或至少为 T1c TNBC 的患者提供基于蒽环类和紫杉类的新辅助治疗方案。

关于在 TNBC 患者中将卡铂添加到基于蒽环类的标准新辅助化疗方案中的共识较少。在高危患者中,在紫杉醇和 AC(多柔比星和环磷酰胺)或 EC(表柔比星和环磷酰胺)的标准新辅助化疗方案中加入铂已被证明可以提高 pCR 率,高达 20%。 荟萃分析在 9 项 RCT(2,109 名患者)中评估了 TNBC 患者中铂类新辅助化疗与无铂新辅助化疗的安全性和有效性,例如,铂类新辅助化疗将 pCR 率从 37.0% 显着提高至 52.1%(几率比率 [OR],1.96;95% CI,1.46 至 2.62,P < 0.001)。使用基于铂的新辅助化疗观察到的 3 级和 4 级血液学不良事件的风险显着更高。研究者在研究 TNBC 中铂类新辅助化疗的 RCT 荟萃分析中发现类似的 pCR 率增加。与不含铂的新辅助化疗相比,含卡铂或顺铂的新辅助化疗显着提高了 pCR 率(相对风险 [RR],1.45;95% CI,1.25 至 1.68;P <0 .0001)。
然而,添加铂类药物对 DFS 和 OS 等长期结果的影响不太确定。没有一项相关试验有足够的效力来评估生存结果。在 CALGB 40603中,卡铂显著改善了乳房或腋窝的 pCR(54% vs 41%,P=0.0029)在 II-III 期 TNBC 患者中加入每周紫杉醇 12 周,然后每 2 周一次 AC,共四个周期。在接受卡铂治疗的患者中,≥ 3 级血小板减少症和中性粒细胞减少症更常见;由于毒性,这些患者也更有可能需要调整剂量、跳过剂量或提前停止治疗。与中位 3 年随访时未达到 pCR 的患者相比,达到 pCR 的患者的无事件生存期和 OS 有所改善。然而,在标准新辅助化疗方案中加入卡铂后,生存结果没有改善。
GeparSixto 随机 II 期临床试验包括 II 期或 III 期 HER2 阳性(n = 273)或 TNBC(n = 315)患者。患者每 21 天接受 18 周新辅助每周紫杉醇、每周非聚乙二醇化脂质体多柔比星和贝伐珠单抗,并被随机分配到同步每周卡铂或不进行额外治疗。这些谁接受卡铂曾在PCR(卡铂的pCR 53.2%的改善 vs 36.9%,无卡铂,P = 0.005)。接受卡铂的患者中止治疗的频率高于未接受卡铂的患者(48% vs 39%)。
有研究者报告了一项 III 期、双盲、安慰剂对照试验(BrighTNess)的结果,该试验评估了添加聚(ADP-核糖)聚合酶(PARP)抑制剂、veliparib 和卡铂或单独使用卡铂的情况对 II-III 期 TNBC 患者进行标准的基于紫杉类的新辅助化疗,然后进行 AC。该研究将 316 名患者随机分配到紫杉醇加卡铂加维利帕利组;160 名患者接受紫杉醇加卡铂;158 名患者单独使用紫杉醇。接受紫杉醇和卡铂治疗的患者的 pCR 率为 58%;在接受紫杉醇、卡铂和维利帕利的患者中为 53%;在单独接受紫杉醇的患者中为 31%。后两组差异有统计学意义(P< 0.0001)。接受卡铂治疗的患者出现 3 级或 4 级毒性(如贫血、中性粒细胞减少和血小板减少)的频率更高。无事件生存期和 OS 是该试验的次要终点,尚未报告。
使用免疫检查点抑制剂治疗早期 TNBC。研究免疫疗法在许多实体瘤中的有效性和安全性越来越受到关注,其中包括乳腺癌。帕博利珠单抗 和阿替利珠单抗都在转移性环境中进行了研究,并且阿替利珠单抗被 FDA 批准用于 PD-L1 阳性 TNBC 的一线治疗,并且几项 II 期试验表明 pCR 率增加。两项 III 期随机临床试验,这些试验涉及免疫检查点抑制剂在治疗非转移性 TNBC 中的作用。KEYNOTE-522 随机、双盲、III 期试验评估了卡铂或紫杉醇联合或不联合派姆单抗,随后 AC 联合或不联合派姆单抗在 II 期或 III 期 TNBC 患者中的应用。在中位随访时间为 15.5 个月的第二次中期分析中,数据显示在卡铂或紫杉醇基础上加入派姆单抗可显着提高 pCR 率。帕博利珠单抗加新辅助化疗组 pCR 患者的百分比为 64.8%(401 名患者中的 260 名),而安慰剂加新辅助化疗组为 51.2%(201 名患者中的 103 名;估计治疗差异,13.6 个百分点;95% CI , 5.4 至 21.8; P< 0.001)。研究人员还报告了两组的初步无事件生存率,最终分析需要 327 个预期事件中的 104 个。对于接受帕博利珠单抗化疗的患者,在 18 个月时存活且无疾病进展而无法进行根治性手术、无局部或远处复发且无第二原发肿瘤的患者的估计百分比为 91.3%(95% CI,88.8 至 93.3)组,安慰剂化疗组的患者为 85.3%(95% CI,80.3 至 89.1)。帕博利珠单抗化疗组和安慰剂化疗组的 3 级或更高级别的治疗相关不良事件分别发生在 76.8% 和 72.2% 的患者中。两个治疗组中最常见的 3 级或更高的不良事件是贫血、中性粒细胞减少、发热性中性粒细胞减少和中性粒细胞计数减少。在接受派姆单抗治疗的患者中,甲状腺功能减退、甲状腺功能亢进和肾上腺功能不全更常见。
IMpassion031 随机、双盲、III 期新辅助治疗试验在早期 TNBC 患者中评估了 阿替利珠单抗 与安慰剂联合白蛋白结合型紫杉醇随后 AC。分析表明,无论患者的 PD-L1 状态如何,将阿替利珠单抗添加到白蛋白结合型紫杉醇后进行 AC显著提高了 pCR 率:在 阿替利珠单抗加化疗组的 165 名患者中有 95 名观察到 pCR(58%;95% CI,50至 65)与安慰剂加化疗组 168 名患者中的 69 名(41%;34 至 49;率差异 17%,95% CI,6 至 27;单侧P=0.0044)。该试验对长期生存结果(无事件生存和 OS)没有把握。阿替利珠单抗加化疗组 37 例(23%)患者和化疗加安慰剂组 26 例(16%)患者发生严重的治疗相关不良事件。两个治疗组之间常见的(≥ 20% 发生率)不良事件相似,并且主要由化疗效果驱动。
新辅助治疗方案的选择应与疾病的分期和亚型相适应。在临床试验之外,TNBC 的新辅助治疗方案反映了辅助治疗方案,并且通常涉及同时使用蒽环类和紫杉类的多化学疗法。在紫杉烷成分期间添加铂类药物可提高 pCR 率,因此可考虑用于高临床风险,例如淋巴结阳性疾病;然而,尚不清楚添加铂是否能改善侵入性 DFS 或 OS。在低风险患者或有心脏危险因素的患者中,蒽环类药物的相关风险可能更甚,可替代基于紫杉烷的方案,如多西紫杉醇加环磷酰胺或卡铂,治疗 6 个周期。在 TNBC 化疗中加入免疫检查点抑制剂可能会增加 pCR,尽管在新辅助治疗中接受这些药物的患者的长期结果和毒性仍在评估中。
对于 HR 阳性/HER2 阴性乳腺癌患者,推荐什么新辅助治疗?

(1)任何 HR 阳性/HER2 阴性乳腺癌患者都可以使用新辅助化疗代替辅助化疗,这些患者无需手术病理数据和/或肿瘤特异性基因组检测即可做出化疗决定。
(2)对于 HR 阳性/HER2 阴性疾病的绝经后患者,可以提供芳香酶抑制剂的新辅助内分泌治疗,以增加局部治疗选择。若无手术意向,可采用内分泌治疗控制疾病。
(3)对于 HR 阳性/HER2 阴性早期疾病的绝经前患者,不应在临床试验之外常规提供新辅助内分泌治疗。
HR阳性/HER2阴性乳腺癌患者的新辅助化疗。没有来自随机 III 期临床试验的直接证据可以为 HR 阳性/HER2 阴性乳腺癌患者的最佳新辅助化疗方案提供建议。对于任何 HR 阳性/HER2 阴性疾病患者,可使用新辅助化疗代替辅助化疗的建议是基于具有里程碑意义的 NSABP B-18 试验数据的推断。结果表明,在手术前或手术后随机分配到 AC 的 II 期或 III 期乳腺癌患者中,辅助治疗和新辅助治疗在 DFS 或 OS 方面没有差异。一般来说,用于指导辅助全身治疗决策的相同患者和疾病因素(例如,淋巴结状态、肿瘤分级和合并症)可用于选择新辅助化疗的 HR 阳性/HER2 阴性患者是合适的。然而,认识到某些因素(如淋巴结状态)可能在某些患者的根治性手术后得到更好的评估。如免疫组织化学标志物(如 Ki67)和基因组预测因子(如 Onco type )在新辅助治疗中,Dx 复发评分尚未确定,这些标志物不应常规用于确定手术和全身治疗的顺序。
绝经后 HR 阳性/HER2 阴性乳腺癌患者的新辅助内分泌治疗。一些研究跟荟萃分析为绝经后 HR 阳性/HER2 阴性乳腺癌患者的新辅助内分泌治疗问题提供了信息。IMPACT(即刻术前阿那曲唑、他莫昔芬或联合他莫昔芬)双盲临床试验将 330 名患有雌激素受体阳性(ER 阳性)、非转移性、侵袭性、可手术的乳腺癌的绝经后女性随机分配到阿那曲唑新辅助治疗组(n = 113) 、他莫昔芬(n = 108)或阿那曲唑和他莫昔芬的组合(n = 109)。在肿瘤客观反应、试验的主要终点(阿那曲唑,37%;他莫昔芬,36%;联合用药,39%)方面,三个治疗组之间没有统计学显著差异。手术结果数据分析显示,在最初被认为需要乳房切除术的患者中,外科医生认为在接受阿那曲唑治疗后适合 BCS 的患者比例 (46%) 与使用他莫昔芬 (22%,P =0. 03)。研究者比较了随机分配的患者接受新辅助内分泌治疗(阿那曲唑或依西美坦)或化疗(多柔比星和紫杉烷)3 个月,并显示出相同的临床客观反应率(两组均为 64%)、pCR(3% vs 6%),内分泌治疗组的保乳手术率略高(33% vs 24%,P = 0.058)。
对 20 项前瞻性随机临床试验(3,490 名患者)进行了基于文献的荟萃分析,以评估新辅助内分泌治疗对 ER 阳性乳腺癌患者的临床反应率和 BCS 率的影响。荟萃分析中的试验必须至少包括一个新辅助内分泌治疗组。主要终点是反应率,尽管作者还在报告时提取了 pCR 和 BCS 率的数据。20 项试验中有 18 项仅包括绝经后妇女;一种包括绝经前妇女和绝经后妇女;一项试验只包括绝经前妇女。根据对七项试验结果的分析,新辅助芳香酶抑制剂比他莫昔芬更有效(更好的临床反应率和 BCS 率)。内分泌单药治疗和双内分泌治疗之间的临床反应率没有观察到差异。荟萃分析还表明,基于芳香酶抑制剂的新辅助内分泌单药治疗的反应率和 BCS 率与联合新辅助化疗观察到的反应率和 BCS 率相当。在所检查的三项研究中,新辅助化疗组的毒性明显更高。
绝经前 HR 阳性/HER2 阴性乳腺癌患者的术前内分泌治疗。系统评价确定了两项随机临床试验,这些试验调查了可手术的 HR 阳性/HER2 阴性乳腺癌绝经前妇女的术前内分泌治疗。他莫昔芬或瑞宁得与醋酸戈舍瑞林联合的研究,以比较新辅助他莫昔芬加戈舍瑞林(n = 99)与新辅助阿那曲唑加戈舍瑞林(n = 98)在 ER 阳性绝经前妇女中的疗效和安全性(STAGE)。早期乳腺癌在接受阿那曲唑加戈舍瑞林的组中,98 名患者中有 69 名 (70.4%) 出现完全或部分缓解,而接受他莫昔芬加戈舍瑞林组的 99 名患者中有 50 名 (50.5%) 出现完全或部分缓解(估计组间差异为 19.9%、95 % CI,6.5 至 33.3;P =0 .004)。在生活质量测量中没有观察到显著差异,尽管该研究没有能力检测到这些结果测量的差异。84% 的患者报告了与治疗相关的不良反应,而他莫昔芬组的这一比例为 77%。然而,辅助试验报告说,与单独使用他莫昔芬相比,内分泌治疗抑制卵巢功能与长期使用相关的毒性更大。
在一项随机 III 期研究中,研究者将 24 周的新辅助化疗与使用他莫昔芬和戈舍瑞林的新辅助内分泌治疗进行了比较。该研究的主要终点是通过卡尺测量和 MRI 确定的临床反应率。最终分析包括 174 名患者。使用卡尺测量 (83.9% vs 71.3%, P = 0.046) 和 MRI (83.7% vs 52.9%, P <0.001)接受化疗的患者的反应率显著更高。化疗组 19 名患者报告了 3 级或更严重的治疗相关毒性,内分泌治疗组没有报告。
不适合化疗或手术的 HR 阳性/HER2 阴性乳腺癌患者的新辅助内分泌治疗。没有随机临床试验的直接证据表明 HR 阳性/HER2 阴性乳腺癌患者不适合化疗或手术或拒绝接受这些治疗方案的内分泌治疗问题。对不适合接受化疗或手术的 HR 阳性/HER2 阴性患者进行有或无手术意图的内分泌治疗的建议代表了专家小组基于乳腺癌管理个人经验的最佳临床意见,不打算手术的内分泌治疗通常只用于不适合手术且医学上不适合化疗的患者。在这种情况下,ASCO 的老年评估 (GA) 指南强调了使用正式的 GA 和预期寿命工具评估老年患者潜在健康状况的重要性,以帮助指导有关化疗的决策。
对于 HR 阳性/HER2 阴性患者,如果肿瘤分期不考虑手术时机,则可给予新辅助化疗;在这种情况下,应使用与手术后考虑的相同的方案。如果需要手术切除的病理信息(即淋巴结状态)或基因组谱来确定化疗是否合适,则不应使用新辅助化疗。尚未对使用基因组分析确定新辅助化疗与新辅助内分泌治疗进行严格研究,因此不推荐使用。绝经后妇女使用芳香酶抑制剂的新辅助内分泌治疗与化疗具有相似的活性,可考虑用于需要肿瘤降期的较大肿瘤;然而,显着的病理反应是罕见的。在绝经前妇女中对新辅助内分泌治疗的研究不那么严格,但现有数据表明,如果需要降期,新辅助内分泌治疗可能不如化疗有效。新辅助内分泌治疗的最佳持续时间尚不清楚,因此应个体化并通过仔细评估患者的临床状态和随时间推移的临床反应来指导。大多数报告采用新辅助内分泌治疗使肿瘤降期的研究进行了 3-6 个月的治疗。
对于 HER2 阳性疾病患者,推荐什么新辅助治疗?

(1)淋巴结阳性或高危淋巴结阴性、HER2 阳性疾病的患者应接受蒽环类和紫杉类或非蒽环类药物联合曲妥珠单抗的新辅助治疗。在新辅助治疗中,帕妥珠单抗可与曲妥珠单抗联合使用。
(2)T1a N0 和 T1b N0、HER2 阳性疾病患者不应在临床试验之外常规接受新辅助化疗或抗 HER2 药物。
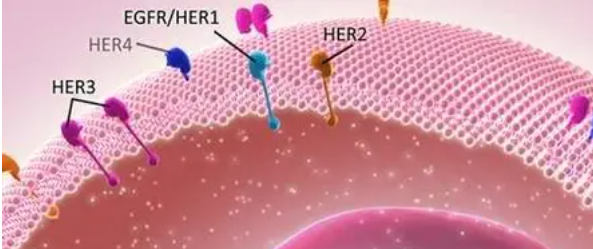
淋巴结阳性或高危淋巴结阴性、HER2 阳性疾病患者的新辅助治疗。淋巴结阳性或高危淋巴结阴性、HER2 阳性乳腺癌患者新辅助治疗的 Meta 分析和 RCT 支持使用基于蒽环类药物的化疗方案和曲妥珠单抗,联合或不联合帕妥珠单抗用于双重抗 HER2 阻断(ACTH±P); 或使用非蒽环类化疗和曲妥珠单抗,同样,有或没有帕妥珠单抗(TCH ± P)。单药曲妥珠单抗研究的 Meta 分析一致证明了将这种药物加入新辅助化疗的优势。在对两个 III 期 RCT 数据的汇总分析中,据报道,在蒽环类紫杉烷化疗中加入曲妥珠单抗可提高 pCR 率,范围为 20% 至 43%(RR,2.07;95% CI,1.41 至 3.03;P = 0.0002),并降低复发率,范围从 20% 到 12%(RR,0.67;95% CI,0.48 到 0.94)。von Minckwitz 等人,在一项将曲妥珠单抗纳入四组(共 614 名 HER2 阳性患者)的汇总分析中发现,在新辅助化疗期间接受曲妥珠单抗治疗的 HER2 阳性乳腺癌患者的 pCR 几率增加了 3.2 倍( P<0.001)。然而,没有观察到曲妥珠单抗周期数与 pCR 率之间存在关联(OR,1.20;95% CI,0.79 至 1.81;P = 0.39)。
Meta 分析还显示,与单药抗 HER2 治疗相比,双重抗 HER2 抑制联合新辅助化疗显着提高 pCR 率。例如,进行了一项网络荟萃分析,该分析结合了 10 项研究(7 个不同治疗组中的 2,247 名患者)的数据,以评估新辅助治疗对 HER2 阳性乳腺癌的安全性和有效性。研究的抗 HER2 药物是拉帕替尼、曲妥珠单抗和帕妥珠单抗。这些作者发现各种双重靶向治疗组之间没有统计学上的显着差异;但是,与其他治疗组相比,双靶向组患者的 pCR 率在统计学上显著更高(OR,2.29;95%CI = 1.02 至 5.02;P =0 .02)。得出的结论是,对于在新辅助治疗中治疗的 HER2 阳性乳腺癌,抗 HER2 药物加化疗的双重靶向证明比单独化疗、单抗 HER2 靶向联合化疗或双重靶向不联合化疗的患者获得 pCR 的数量在统计学上显着更多化疗。在对该网络荟萃分析的更新分析中结合了 13 项研究(7个不同治疗组中的 3,160 名患者)的数据,证实在新辅助治疗中,两种抗 HER2 药物和化疗的组合对 HER2 阳性乳腺癌最有效。最近,在可手术的 HER2 阳性乳腺癌的新辅助治疗中,评估了曲妥珠单抗联合帕妥珠单抗与单独曲妥珠单抗联合化疗的疗效和安全性。
通过为指南进行的文献检索确定的个别 RCT,除了少数例外,都包含在一项或多项审查的荟萃分析中,此处不再进一步总结。综合考虑,这些试验的数据支持使用基于蒽环类的化疗方案加曲妥珠单抗,或使用非蒽环类化疗和曲妥珠单抗,在淋巴结阳性或高危淋巴结阴性、HER2 阳性疾病患者中。专家小组进一步认识到,在这些方案中加入帕妥珠单抗是一种选择(ACTH ± P 或 TCH ± P)。这是基于从NeoSphere,新辅助培妥珠单抗和曲妥单抗的随机II期试验的数据和随后的加速,FDA在新辅助批准。尽管添加帕妥珠单抗导致 pCR 增加,但应注意的是,辅助设置中的验证性 APHINITY 试验导致整个研究人群的侵入性 DFS 略有改善。这种效果在淋巴结阳性人群中最为明显,加入帕妥珠单抗后,侵袭性 DFS 改善了 4.5%。
随机、开放标签 II 期 NeoSphere 试验比较了曲妥珠单抗加多西他赛(A 组,n = 107)与帕妥珠单抗和曲妥珠单抗加多西他赛(B 组,n = 107)与帕妥珠单抗和曲妥珠单抗(C 组,n = 107)与帕妥珠单抗的对比在新辅助治疗的局部晚期、炎症性或早期 HER2 阳性乳腺癌女性中,联合多西他赛(D 组,n = 96)给药 12 周,然后接受基于蒽环类药物联合曲妥珠单抗的方案。乳房中的pCR 是主要试验终点。结果表明,与接受曲妥珠单抗联合多西他赛的患者(107 名患者中的 31 名;29.0%)相比,接受帕妥珠单抗和曲妥珠单抗联合多西他赛的患者 pCR 率显着提高(107 名患者中的 49 名;45.8% [95% CI,36.1 至 55.7]) [20.6 至 38.5];P = 0.0141)。发热性中性粒细胞减少症和白细胞减少症是最常见的 3 级或更高级别的不良事件。A、B 和 D 组的严重不良事件比例大致相同(10%-17% 的患者);C 组,即最初未接受细胞毒性治疗的患者,pCR 率最低,严重不良事件的比例较低(4% 的患者)。在随后的出版物中,报告了 NeoSphere 5 年无进展生存期 (PFS)、DFS 和安全性结果。PFS 和 DFS 结果仅用于描述目的,因为该试验没有能力检测生存结果差异。PFS 和 DFS 的分析显示,与曲妥珠单抗和多西他赛联合帕妥珠单抗相关的长期结果没有静态显着差异。在 NeoSphere 数据的 5 年分析中观察到的安全性特征与主要分析的一致。
随机、多中心、开放标签、III 期 KRISTINE 试验在新辅助治疗中比较了 T-DM1 加帕妥珠单抗与多西他赛、卡铂和曲妥珠单抗加帕妥珠单抗的潜在毒性较低的方案。本研究发现,与接受 T-DM1 加帕妥珠单抗的患者相比,接受含化疗方案(TCH-P)的患者明显更多(55.7% vs 44.4%;P=0 .016)。T-DM1 加帕妥珠单抗组与更少的 3-4 级不良事件和更少的严重不良事件相关,并且与患者报告的与健康相关的生活质量和身体功能的维持时间更长。由于 pCR 率较低,专家组不建议在淋巴结阳性或高危淋巴结阴性、HER2 阳性疾病患者中使用新辅助 T-DM1 加帕妥珠单抗。
新辅助治疗和 T1a N0 和 T1b N0 HER2 阳性乳腺癌患者。T1a 和 T1b 肿瘤患者尚未纳入新辅助治疗试验,因此没有关于这些患者是否受益于新辅助治疗的数据。反对在这些患者中使用新辅助治疗的建议部分代表了专家小组根据个人乳腺癌管理经验得出的最佳临床意见,这表明在该组中,新辅助治疗与辅助治疗相比几乎没有额外临床益处的潜力,并担心过度治疗。对过度治疗的担忧是基于多中心 II 期辅助紫杉醇和曲妥珠单抗 (APT) 试验的结果,该试验对 406 名淋巴结阴性患者 (98.5%) 每周给予紫杉醇和曲妥珠单抗 12 周,然后是 9 个月的曲妥珠单抗, HER2 阳性乳腺癌,49。3 年时,分析显示早期疾病复发的风险 < 2%;无侵袭性疾病的生存率为 98.7%(95% CI,97.6 至 99.8)。APT的试验的长期结果发表在2019年的7年癌特异性存活率乳房为98.6%。
T1c N0 疾病患者存在不确定性,因为这些患者被纳入 APT 降阶梯试验和 KATHERINE 试验。根据临床情况,这些患者可以考虑接受新辅助化疗。优点是如果患者没有 pCR ,T-DM1 可能会带来额外的好处;然而,根据 APT 的结果,存在过度治疗的风险。
独立于细胞毒性化疗主干,将曲妥珠单抗单独加入新辅助化疗可使 pCR 率提高 2 至 3 倍,并且是 HER2 定向治疗的基础。添加第二种 HER2 靶向治疗进一步提高了 pCR 率,但绝对获益各不相同,HR 阴性疾病和淋巴结阳性疾病的患者似乎获益最多。HER2 阳性乳腺癌的治疗体现了采用升级和降级策略定制治疗的目标。在新辅助治疗中,HER2 靶向治疗联合化疗,如果发现残留病灶,则继以 T-DM1 辅助治疗,说明高危疾病的适当升级。相比之下,APT 方案在 I 期疾病的辅助治疗中的应用表明目前实施的降阶梯治疗。正在进行的研究将继续阐明新辅助治疗中的其他降阶梯方法。
-----------END--------------
参考文献(滑动查看)
[1] Rubens RD, Sexton S, Tong D, et al: Combined chemotherapy and radiotherapy for locally advanced breast cancer. Eur J Cancer 16:351-356.
[2] Fisher B, Brown A, Mamounas E, et al: Effect of preoperative chemotherapy on local-regional disease in women with operable breast cancer: Findings from National Surgical Adjuvant Breast and Bowel Project B-18. J Clin Oncol 15:2483-2493.
[3] Schmid P, Cortes J, Pusztai L, et al: Pembrolizumab for early triple-negative breast cancer. N Engl J Med 382:810-821, 2020.
[4]Spring LM, Fell G, Arfe A, et al: Pathologic complete response after neoadjuvant chemotherapy and impact on breast cancer recurrence and survival: A comprehensive meta-analysis. Clin Cancer Res 26:2838-2848.
声明:本文由好医术肿瘤学院作者编辑,仅供学习交流,如有侵权请联系删除,转载需授权。













