
急性冠脉综合征(ACS)包括不稳定心绞痛(UA)、非ST段抬高型心肌梗死(NSTEMI)与ST段抬高型心肌梗死(STEMI),多是由冠脉内动脉粥样硬化斑块破裂或侵蚀相关的血栓阻塞所致。ACS是一种常见病、多发病,而且是心血管系统中的危急重症,与严重的不良预后相关,所以需要迅速启动有效的专业治疗。STEMI患者一般是发生了单支或多支冠脉的完全阻塞。NSTEMI与UA(合称为非ST段抬高型ACS[NSTE-ACS])的发病机制与急性冠脉血栓相似,两者实为同一种疾病的不同临床表现,均是由冠脉中斑块形成、脂质沉积,可导致冠脉管腔减小,严重限制心肌供血。
NSTE-ACS相关血栓中多富含血小板,而导致STEMI患者冠脉完全阻塞的血栓则富含纤维蛋白。血小板及其他血栓成分可引起NSTEMI患者的远端栓塞,导致冠脉微循环阻塞及进一步的心肌缺血和坏死。
NSTE-ACS诊断
三种ACS患者的临床表现可完全相同,ACS患者通常存在以下特征:
1. ACS患者的典型胸痛特征
①静息时长时间心绞痛(>20分钟)
②新发心绞痛(日常活动明显受限)
③既往稳定性心绞痛近期不稳定,至少CCSⅢ级心绞痛特征
④心梗后心绞痛持续时间更长、发作更频繁
⑤存在血流动力学不稳定相关胸痛
⑥存在恶心、呕吐、晕厥或发汗相关的胸痛
2. 冠心病存在的血管危险因素
吸烟、高血压、糖尿病、血糖耐量受损、肥胖、缺血性心脏病史、<55岁一级亲属曾发生ACS、男性、年龄、绝经提前、种族。
3. NSTE-ACS相关心电图改变
至少两个连续导联中ST段压>0.5mm(0.05mV)提示NSTE-ACS,与患者预后相关(ST段压低>1mm与年死亡或后续心梗风险11%相关),心前导联中有较深且对称的T波导致>2mm。(如图)
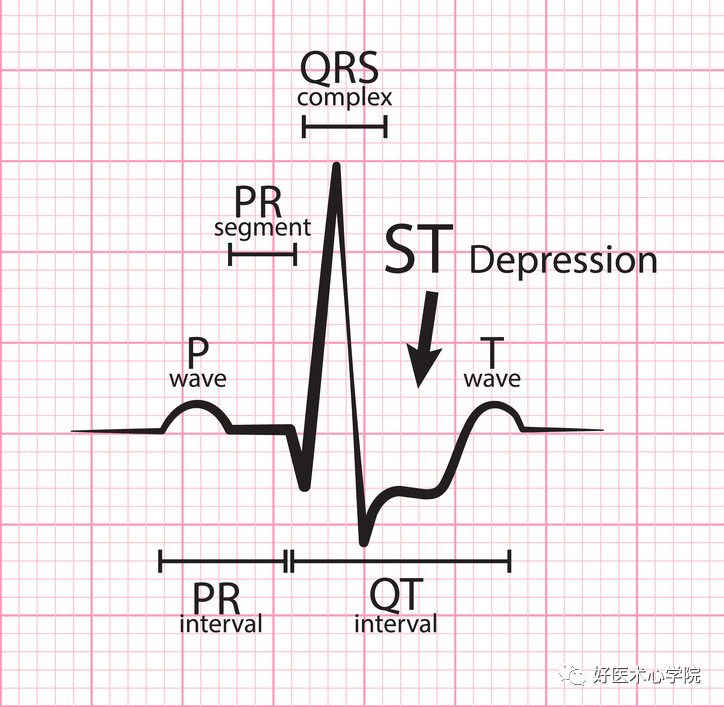
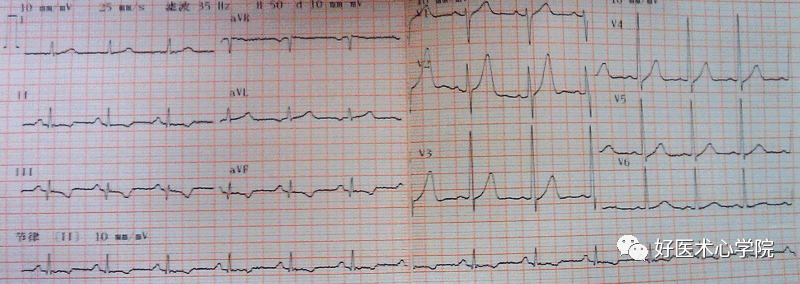
注意:
当STEMI患者的某支冠脉血管发生突然急性闭塞,心电图即表现为ST段抬高;
NSTE-ACS在胸痛时表现出ST段压低,此时患者可能只发生心绞痛而无心梗,或是发生心梗与多支多处血管病变,比STEMI更为复杂。
对于NSTE-ACS患者,在得出血检结果之前无法确诊UA(典型症状及心电图改变,无标志物升高)或NSTEMI(肌钙蛋白阳性)。稳定性患者及每次胸痛发作时可定期(例如每6~24小时)重复12导联心电图检查。
约5%的NSTE-ACS患者心电图结果正常。若患者存在疑似ACS病史,即便其心电图检查正常,也应立即转院进行专业的评估和治疗。
NSTE-ACS的诊断及分诊的临床路径:
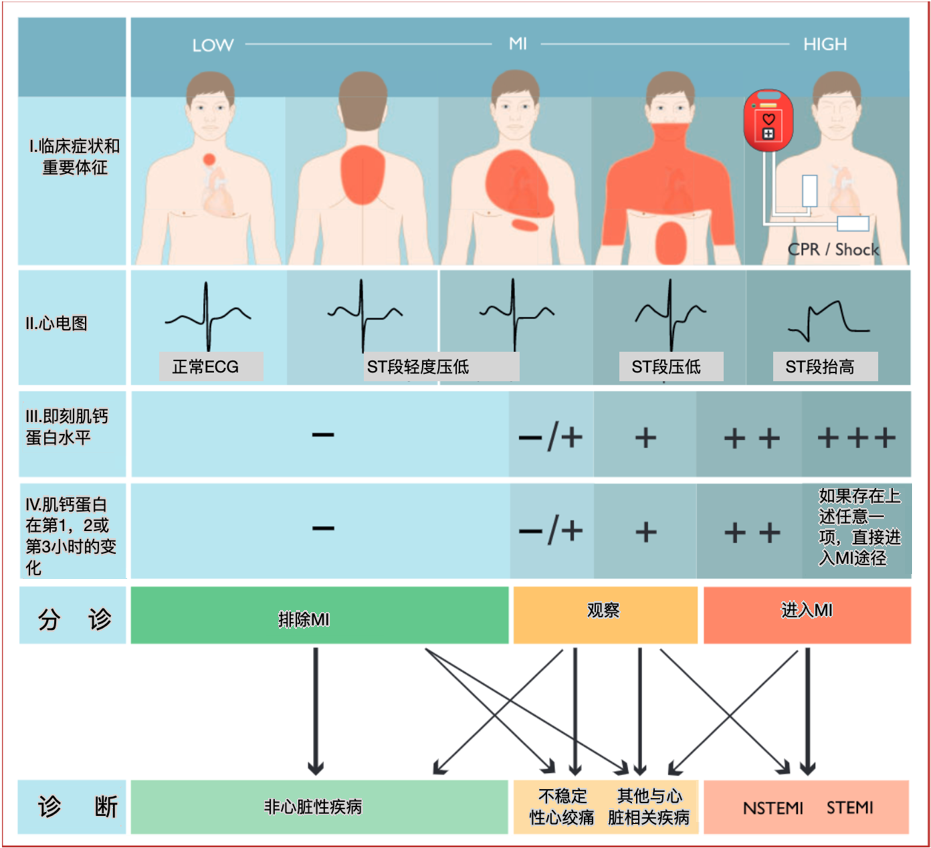
关于NSTEMI与STEMI的鉴别
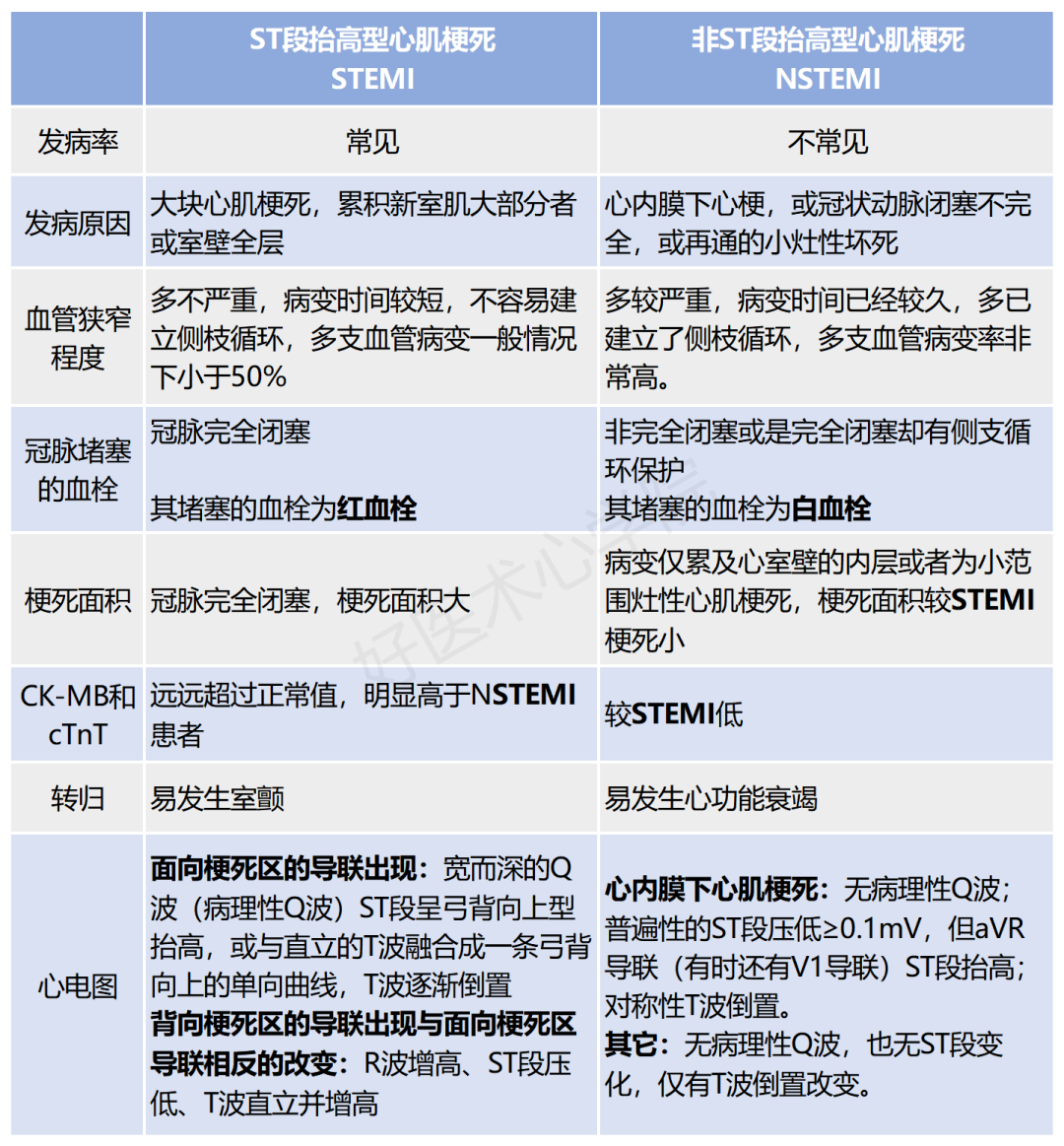
注:
-
红血栓又称红细胞血栓,主要是由纤维蛋白与红细胞组成,溶栓为这类血栓的最佳治疗方案;
-
白血栓亦称血小板血栓,主要是由于血小板聚集所组成,带有少量纤维蛋白,不含红细胞。主要组成成分是血小板和胶原纤维,治疗这类血栓主要采用的是针对血小板聚集的药物,如阿司匹林。
ACS危险分层
尽管不同患者的临床表现相似,但其预后可能存在差异。现有的风险评分多涉及临床表现、生化及心电图特征,有助于ACS患者的危险分层并指导治疗,尤其是冠脉介入治疗。
ACS患者心血管风险标志物(基于AHA及ESC指南)
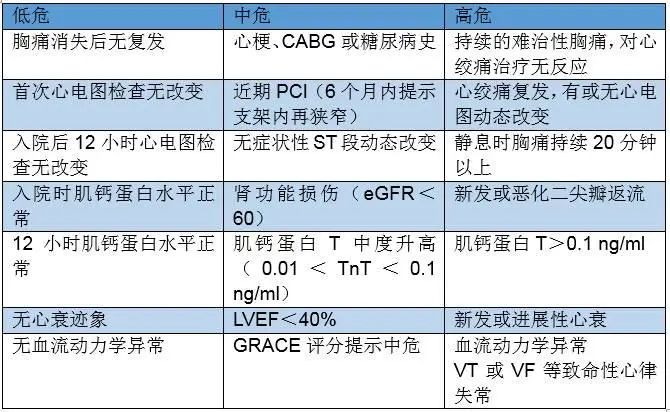
尽管ACS是种很严重的疾病,但部分患者的心血管事件较低,可考虑住院或门诊管理,中危患者应在72~96小时内完成冠脉解剖评估,高危患者则需紧急血管造影及介入治疗。目前有若干评分系统可用于进一步评估主要不良心血管事件(MACE)的风险,临床上最常用的三种危险分层系统包括:TIMI评分、GRACE评分、PURSUIT评分。
NSTE-ACS药物治疗管理
一、常用药物治疗:
*点击图片可放大
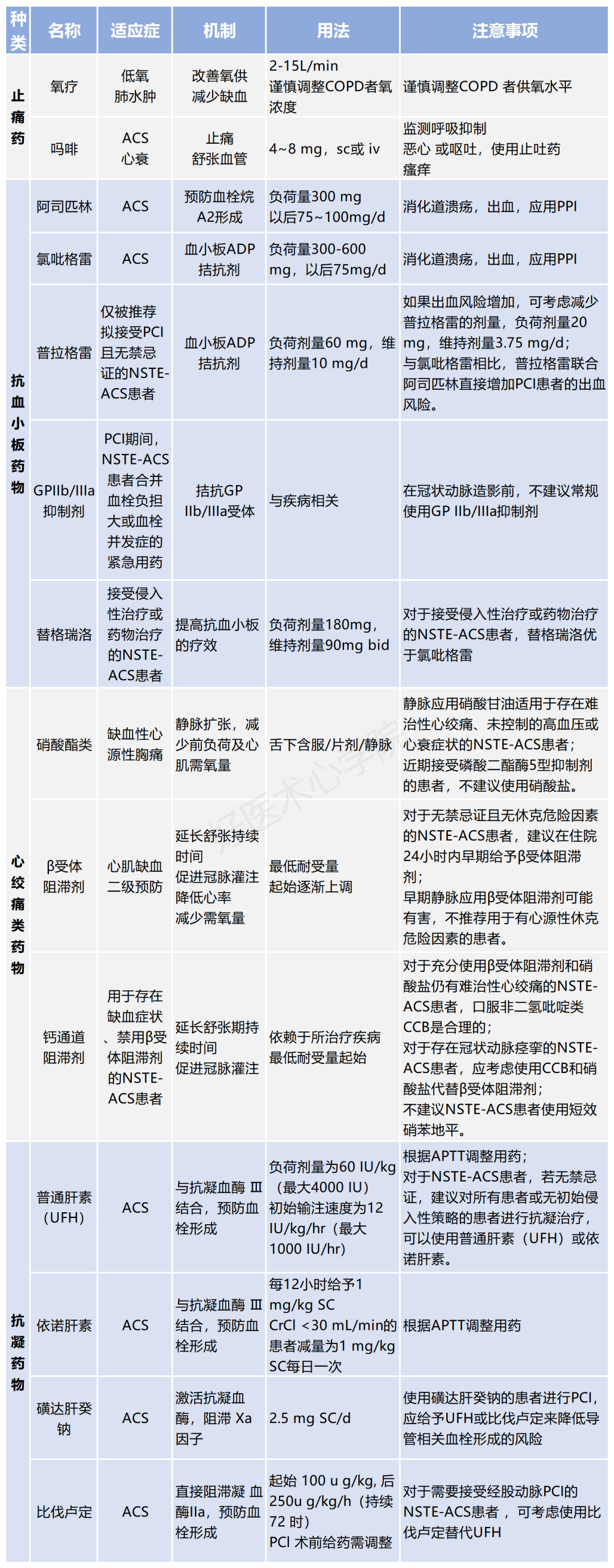
二、其他药物治疗:
1. RAAS抑制剂
①建议所有NSTE-ACS患者在住院期间使用ACEI,除非有禁忌证;
②不耐受的患者建议使用ARB,除非有禁忌证;
③对于无显著肾功能不全或高钾血症、已接收ACEI和β受体阻滞剂的最佳治疗、心衰伴LVEF<40%的NSTE-ACS患者,建议使用醛固酮受体阻断剂,优选依普利酮;
④不建议NSTE-ACS患者联合使用ACEI和ARB。
2.降脂治疗
①建议所有NSTE-ACS在住院期间使用他汀类药物或者他汀类药物联合依折麦布,除非有禁忌证;
②NSTE-ACS患者的LDL-C目标为<70mg/dL;合并糖尿病者,目标可考虑为<55mg/dL。
NSTE-ACS血管重建
NSTE-ACS与STEMI均由血管狭窄与血栓形成所致,因此需要进行再灌注治疗以疏通血管。再灌注治疗同常包括3种方法,即静脉溶栓治疗、介入治疗与冠状动脉旁路术(CABG),但两者在再灌注治疗方面并不完全一致,实践证实静脉溶栓不适用于NSTE-ACS。
对于存在多支血管病变且能清楚识别罪犯病变的NSTE-ACS患者,极高危者应接受PCI,包括血流动力学不稳定、急性肺水肿、快速或缓慢性心律失常、难治性心绞痛伴罪犯动脉闭塞。对于有经验的操作者和桡动脉入路手术量大的中心,推荐使用桡动脉入路进行冠状动脉造影和PCI;推荐接受PCI的患者选用新一代DES。
对于具备紧急CABG的指征的NSTE-ACS患者,无论抗血小板治疗如何,均应进行CABG治疗。对于需要CABG治疗的稳定NSET-ACS患者,可在病情稳定数日且停止双联抗血小板治疗(DAPT)后进行CABG治疗。对于择期CABG患者,术前应停用替格瑞洛至少3天,氯吡格雷至少5天,普拉格雷至少7天。
多数患者不愿接受手术治疗(冠状动脉旁路术),所以大部分患者会选择介入治疗。
1. 介入术前危险分层评估
术前对患者进行危险分层,决定是否进行早期血运重建,推荐采用全球急性冠状动脉事件注册(GRACE)危险评分作为危险分层的首选评分方法。GRACE评分根据Killip心功能分级、收缩压、心率、年龄、肌酐水平、院前有无心脏骤停、ST段压低程度与心肌标志物升高程度对患者危险进行量化,评分越高者院内死亡及出院后6个月内死亡风险越高,此类患者需积极接受再灌注治疗,根据危险分层与指南推荐决定血运重建的时机。
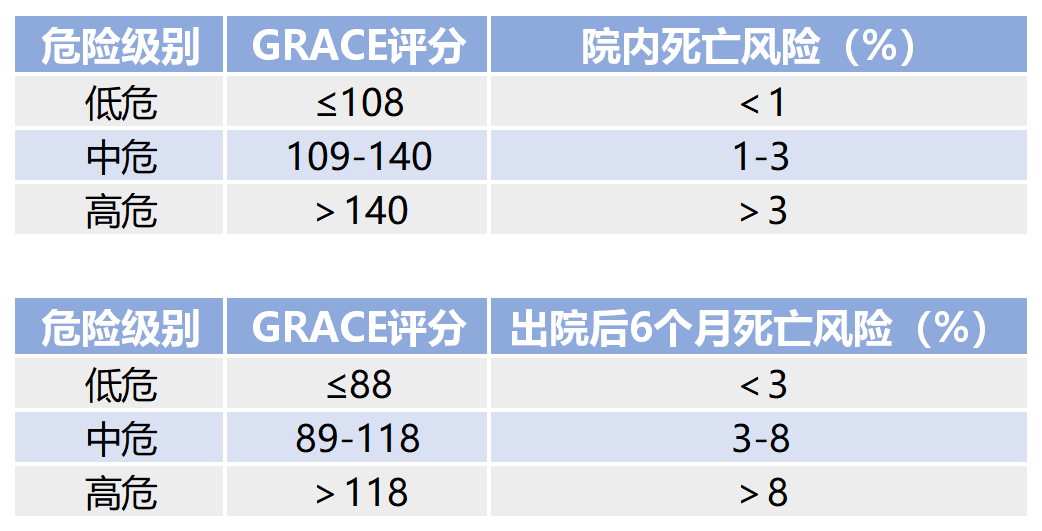
2. NSTE-ACS的介入治疗时机
-
极高危患者GRACE评分>180,通常具有心绞痛伴心衰、血流动力学不稳定、合并严重室性心律失常及持续或反复缺血发作等特征,可能危及生命,需行紧急PCI(2小时内)。
-
高危患者GRACE评分>140,心绞痛发作时间>20分钟,心绞痛反复发作且有加重趋势,心肌缺血发作时心电图ST段压低(>1mm),cTnl/cTnT升高,伴心功能不全,需行早期PCI(24小时内)。
-
中危患者GRACE评分在109~140之间,心电图ST-T改变,cTnl/cTnT轻度升高,医生需明确患者是否存在糖尿病、肾功能不全、左室功能降低、既往心梗、既往PCI或CABG史,行延迟PCI(72小时内)。
-
缺血面积小、无症状的低危患者可进行药物保守治疗,可诱发缺血、缺血面积>左心室10%的患者可择期行CAG或PCI。
约10%的NSTE-ACS患者需要CABG,此类患者通常存在左主干或三支血管病变、合并心功能不全、糖尿病。一般在药物保守治疗至病情稳定后数日(一周)进行CABG。
NSTE-ACS长期管理
1. 二级预防
若无禁忌证,出院后应继续使用ACEI(或ARB)、β受体阻滞剂和他汀类药物(或他汀类药物+依折麦布)。应长期使用阿司匹林,维持剂量为100mg/d。
2. DAPT疗程(双抗治疗)
①对于接受PCI的NSTE-ACS患者,若无出血并发症,应给予P2Y12抑制剂治疗至少12个月。对于高缺血风险的NSTEMI患者,DAPT疗程可超过12个月。DAPT超过12个月者,可考虑给予替格瑞洛60mg bid。
②对于接受CABG的NSTE-ACS患者,术后应恢复P2Y12抑制剂治疗,完成12个月DAPT。
③对于接受药物治疗的NSTE-ACS患者,优先使用替格瑞洛代替氯吡格雷,疗程12个月,不建议使用普拉格雷。
④若12个月DAPT的出血风险超过获益,可考虑提前(<12个月)停用P2Y12抑制剂。
⑤DAPT评分可用于评估延长DAPT的获益。
3. 需要长期口服抗凝的患者
①对于合并房颤、CHA2DS2-VASc≥2分的NSTE-ACS患者,可使用DAPT+NOAC(新型口服抗凝药)的三联治疗1-6个月。
②对于高出血风险的房颤合并NSTE-ACS患者,可使用NOAC+氯吡格雷的双联治疗来替代三联治疗12个月。
③对于房颤合并NSTE-ACS患者,可在NSTE-ACS后1年停用抗血小板药物,继续长期NOAC单药治疗。
④对于高缺血风险或接受复杂PCI手术的房颤合并NSTE-ACS患者,可考虑NOAC+氯吡格雷双联治疗超过12个月。
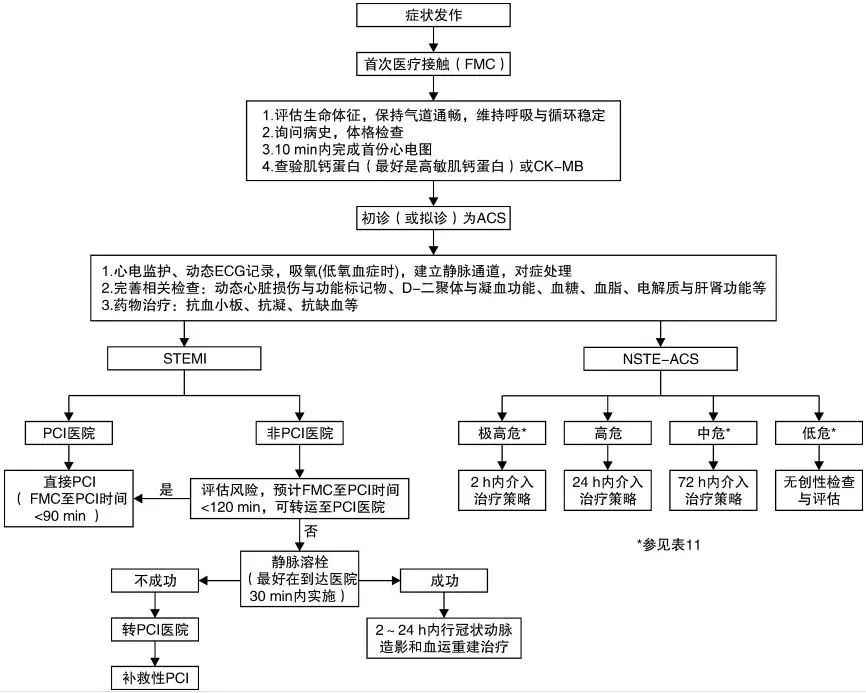
NSTE-ACS诊疗流程













