黏液上皮性卵巢癌
mEOC的治疗主要是外科手术。在第一阶段,保育手术适合年轻患者,包括单侧输卵管卵巢切除术和腹膜分期手术(细胞学,腹膜活检和网膜切除术)。复发的风险低于报告的患有Ⅰ期浆液性癌症的女性。在老年患者中,首选双侧输卵管卵巢切除术。在晚期阶段,应尝试以宏观完整切除为目标的大型手术,然后进行全身治疗。
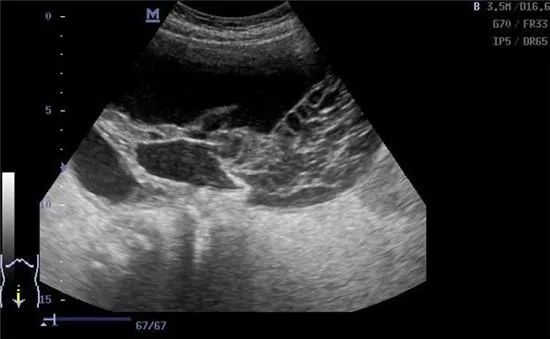
NCCN指南建议仅对IA或IB期mEOC进行手术,并建议采用铂类辅助化疗(紫杉醇/卡铂或奥沙利铂联合氟尿嘧啶或卡培他滨)以治疗更晚期的疾病。
研究表明,mEOC的突变情况不同于浆液性癌。黏液性肿瘤与BRCA突变或同源重组缺陷无关,因此它们不太可能受益于聚ADP核糖聚合酶(PARP)抑制剂。但是,显示可能是可靶向的突变或扩增。在具有野生型KRAS的人表皮生长因子受体2(HER2)阴性肿瘤中,已检测到BRAF,FGFR或STK11中的表皮生长因子受体(EGFR)扩增或突变,表明这些肿瘤可能对靶向疗法有反应。正如不存在的KRAS突变识别的大肠癌患者,临床前研究表明,在mEOC细胞系与野生型西妥昔单抗抑制增殖KRAS,而它在KRAS突变的mEOC模型中没有抗肿瘤作用。
子宫内膜样卵巢癌
子宫内膜样肿瘤是囊性,实体性或出血性的,无乳头状。高度子宫内膜样癌的特征与高度浆液性癌相似,表达为p53,p16和WT1。卵巢子宫内膜样癌最常出现ARID1A(33%),PTEN(32%),CTNNB1(28%),PIK3CA(26%)和KRAS(26%)改变。基本治疗包括完整的细胞减灭术,并进行全面的分期,然后进行辅助治疗或观察。保留生育能力的手术是ⅠA-ⅠC1期肿瘤的一种选择,在这些病例中,一半的复发发生在对侧卵巢,因此可以通过随后的手术抢救。在第一阶段辅助化疗作用的证据很少。根据一些数据,具有ⅠA / ⅠB期,1/2级,已完成手术分期的肿瘤的妇女5年生存率(DFS)超过90%,不需要辅助化疗。患有3级(任何分期)和ⅠC-Ⅱ期肿瘤的患者预后较差,应考虑使用铂类辅助化疗。
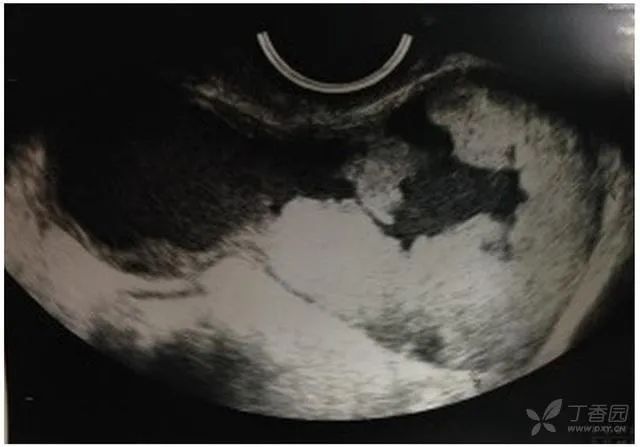
最佳的化疗持续时间尚不确定。GOG-157试验在高危早期EOC中每3周评估了3个周期与6个周期的辅助卡铂和紫杉醇,其中包括25%的子宫内膜组织学患者。发现接受六个疗程的患者复发风险较低,尽管更长的治疗时间与更大的毒性相关。因此,对于Ⅱ/ Ⅳ期子宫内膜样癌以及高级别浆液性癌,推荐使用六个周期的标准卡铂加紫杉醇/贝伐单抗治疗。
总体而言,研究在使用的内分泌药物(他莫昔芬,来曲唑,阿那曲唑,依西美坦等)的类型上有很大差异,并且组织学亚型/ ER表达阈值定义不明确。但是,对于内分泌治疗的反应,激素受体的阳性状态和组织学亚型似乎是相关的。在涉及2490例患者的荟萃分析中。研究发现,接受内分泌治疗的EOC患者的临床获益率为41%,这表明有一部分肿瘤生物学患者对治疗反应良好。他莫昔芬的临床获益率最高(43%),而芳香酶抑制剂为39%。基于这一证据,NCCN指南建议在1级子宫内膜样肿瘤患者的辅助和复发治疗中进行激素治疗(推荐2B)。
癌肉瘤
卵巢癌肉瘤是一种罕见的肿瘤,由恶性上皮和间质组成。据估计,癌肉瘤占所有EOC的1-4%。诊断为癌肉瘤的患者是在呈现的时间显著老,更经常本晚期疾病,和相对于其他EOC亚型时具有更短的OS。
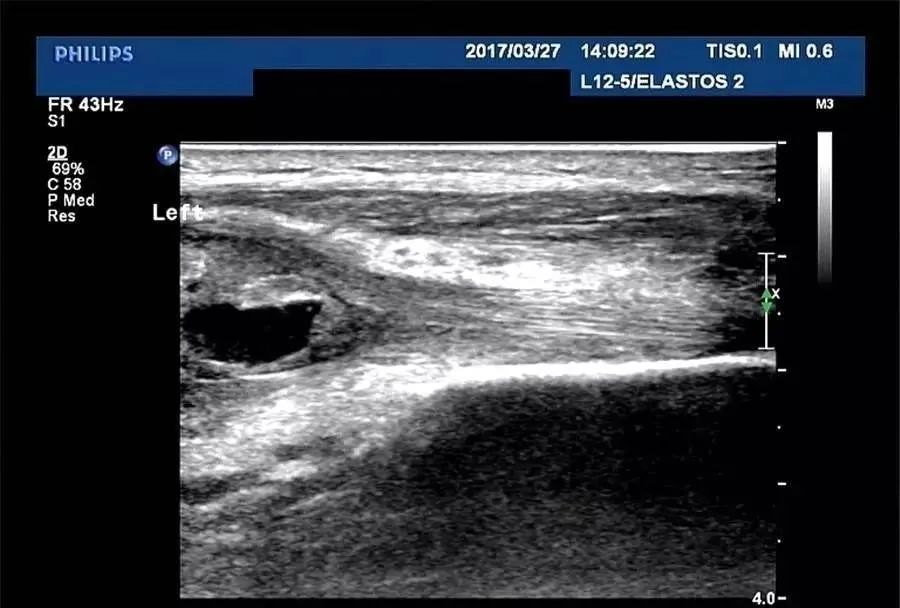
尽管由于癌肉瘤患者通常不包括在RCT中,所以前瞻性证据有限,但癌肉瘤的治疗与其他卵巢肿瘤相似,包括细胞减灭术以及晚期癌症妇女的辅助化疗。用于癌肉瘤的治疗方案包括铂,紫杉醇,异环磷酰胺,阿霉素和达卡巴嗪作为单药或联合用药。
在没有RCT的情况下,并且在已证明卡铂和紫杉醇联合使用可有效治疗EOC的前提下,指南建议采用该方案治疗癌肉瘤。研究数据发现,一线卡铂在患有原发性卵巢癌的女性(n = 26)中的OS达到27.1个月,RR达到72%。另一例包括50例癌肉瘤患者的病例对照研究报告,用卡铂和紫杉醇治疗时,RR的中位数为62%,OS的中位值为24个月(95%CI,18-29),尽管这低于其他EOC中的观察结果。亚型。顺铂和异环磷酰胺的组合已被证明对治疗子宫癌肉瘤有效,在一项小规模研究中,它也已被用于卵巢肿瘤,甚至比紫杉醇/卡铂获得更好的疗效。
恶性卵巢生殖细胞肿瘤(MOGCT)
MOGCT起源于原始生殖细胞和性索-基质衍生物,包括营养不良,不成熟畸胎瘤,胚胎性肿瘤,非妊娠性绒毛膜癌和内膜窦(卵黄囊)肿瘤。MOGCT占所有卵巢恶性肿瘤的3–5%,并且在年轻女性和少女中更常见。
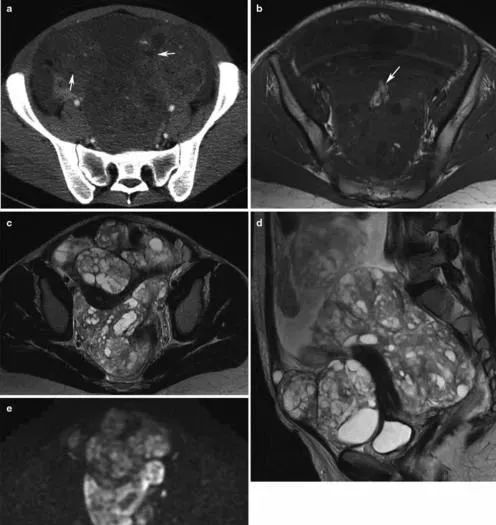
与EOC不同,MOGCT通常表现为腹部症状,包括疼痛,明显的骨盆肿块和/或由于荚膜扩张,出血和坏死引起的腹水。尽管症状有助于早期诊断,但大多数症状是单方面的,并在I或Ⅱ期得到诊断。推荐的初始检查包括血清肿瘤标志物[甲胎蛋白(AFP),β-人绒毛膜促性腺激素(B-HGC)],胸部X线检查,腹部CT和骨盆超声检查。绒毛膜癌患者的B-HGC升高;发现AFP伴有含有卵黄囊肿瘤成分的肿瘤。胚胎癌可能同时产生两种血清标志物。以及神经营养不良会产生低水平的B-HGC和乳酸脱氢酶(LDH)。
血清标志物在MOGCT的诊断中起着重要作用,并被认为具有预后价值,可用于患者的治疗和随访,表明其已缓解或复发。其他不良的预后因素包括晚期,组织学亚型(非营养不良/未成熟畸胎瘤)和残留疾病。最常见的组织学是dysminminoma,而非妊娠绒毛膜癌和胚胎癌则较少见。
MOGCT在经过多模式联合手术治疗和辅助全身治疗后具有良好的预后,被认为是这些肿瘤的标准治疗方法。手术类型取决于肿瘤的扩展,传统上保留生育能力的手术被认为是可以接受的。它包括单侧输卵管卵巢切除术,腹腔冲洗,仔细和系统地探查腹腔与盆腔及腹腔腹膜,网膜切除术的多点活检,及腹膜后淋巴结清扫术,包括双边盆腔及腹主动脉旁淋巴结区域。全子宫切除术和双侧输卵管卵巢切除术保留给那些病情较严重的患者。
联合化疗已大大改变了MOGCT患者的预后。长春新碱,放线菌素和环磷酰胺是1970年代初期的用药标准。在1990年博来霉素,依托泊苷和顺铂(BEP)成为新标准之前,长春碱,博来霉素和顺铂(PVB)也被认为是另一种有效方案。在生殖细胞睾丸癌患者中,BEP与PVB方案进行了比较,显示出相似的结果。功效显着降低毒性,因此被用于MOGCT妇女的治疗。
建议所有Ⅱ至Ⅳ期恶性营养不良或未成熟畸胎瘤患者进行辅助化疗。Ⅰ期,2至3级未成熟畸胎瘤;以及任何阶段的胚胎肿瘤或内胚窦肿瘤。仅选定的ⅠA或ⅠB期患者可以进行观察。BEP的四个疗程被认为是标准方案,尽管某些低危或Ⅰ期疾病的患者可以接受三个疗程的BEP或三个疗程的依托泊苷/卡铂治疗,尤其是在避免毒性至关重要的情况下。另一种有效的治疗方案是POMB-ACE(顺铂,癌性长春新碱,甲氨蝶呤,博来霉素,放线菌素D ,环磷酰胺,依托泊苷),最初用于睾丸癌患者。与其他方案相比,它具有相似的RR,并且通常具有良好的耐受性。尽管MOGCT的预后良好,但仍有少数病例会复发。由于这些肿瘤的稀有性,对于复发性疾病的治疗通常是从针对睾丸癌制定的方案中推断出来的。
恶性索间质瘤
恶性索间质肿瘤很少见,仅占所有卵巢肿瘤的7%。这些肿瘤起源于原始的性索或基质细胞,最常见的是源自颗粒的肿瘤,其次是Sertoli-Leydig细胞肿瘤。大多数表现为低级且预后良好,在年轻患者中更常见,除了成年的颗粒细胞瘤,其表现较晚(至55岁)。恶性索间质肿瘤由于产生雄激素,雌激素和皮质激素,通常具有激素相关的症状(包括病毒化和雌激素过多)。组织学分类包括纯性脐带瘤,纯基质瘤和混合瘤。在这些肿瘤中可以发现DICER1,STK11和FOXL2中的突变。
主要治疗方法是手术。对于希望保持生育力并患有早期肿瘤(ⅠA或ⅠC期)的患者,建议保留生育力的手术。对于所有其他患者,建议进行完整的分期(腹膜液采样,对侧卵巢检查,腹膜活检和任何可疑病变,网膜活检和淋巴结触诊)。辅助治疗包括放射治疗有限疾病和基于铂的化疗治疗Ⅱ~Ⅳ期疾病。由于它们的稀有性,很少有研究关注辅助治疗的有效性。目前,最常用的化疗方案是BEP 4至6个循环,虽然紫杉醇+卡铂的组合也显示出是有效的方案。
复发并不常见,但是对于那些具有复发性全身疗法的患者,包括单药紫杉烷或紫杉烷与铂化合物或异环磷酰胺联合使用。包括芳香酶抑制剂,他莫昔芬和亮丙瑞林在内的内分泌治疗也已显示出疗效。单独使用贝伐单抗或联合使用贝伐单抗是复发性疾病的另一种治疗选择。
结论
非浆液性EOC代表了异质性和罕见的肿瘤组。其中大多数是在五十多岁的女性中诊断出来的,处于早期阶段,并且与高级别的浆液性肿瘤相比,对常规的铂类化疗方案较不敏感。通常,非浆液性EOC的早期预后较好,但CCC和癌肉瘤除外,它们往往更具侵略性,且生存率较差。另一方面,MOGCT和性索间质肿瘤主要影响年轻患者,辅助化疗后的预后非常好。尽管这些肿瘤很少见,但对于所有为卵巢癌女性提供护理的临床医生而言,了解可用的治疗方案以及未来改善其治疗的潜在策略都是至关重要的。