虽然众多冠心病的临床试验,都把死亡率、心肌梗死、血运重建、中风等作为主要研究终点。但从病理生理学的角度来说,动脉粥样硬化斑块的逆转或者消退,才是ASCVD的终极治疗目标。
虽然我们对动脉粥样硬化的发病机制和治疗手段有了长足进步,临床中也确实有一些零星的个案报道,提示经过积极的血脂管理,动脉粥样硬化斑块可明显逆转。但作为一种慢性疾病,很多人认为现有的治疗手段,仅可以稳定斑块,使其不进展或缓慢进展。似乎斑块逆转和消退是一个「伪命题」,是一项不可能完成的任务。
当然,我们不得不承认,部分斑块确实很难或不可能逆转,比如斑块完全钙化、血管成「陶瓷」样改变的患者。但部分软斑块仍存在这种潜力。在本文中,我们回顾了血管内超声(IVUS)相关的降脂试验,并总结目前积极降脂治疗的有效性,进而探讨该疗法在抑制动脉粥样硬化的进展的同时,是否能诱导消退或逆转。
一、动脉粥样硬化斑块逆转与消退的机制
20世纪以来,医学界一度把通过降低血脂水平使动脉粥样硬化消退,作为一个终极的治疗目标。几项动物实验研究表明,在动物模型中,从高胆固醇饮食转变为低胆固醇饮食后,斑块面积减少,从而显示出斑块消退的可能性。
也有研究显示,改善斑块脂蛋白暴露,可迅速减少斑块内巨噬细胞的含量和泡沫细胞形成,并能降低炎症标志物的表达、诱导抗炎标志物的富集。
斑块消退伴随着斑块微环境的有效改善,特别是血浆载脂蛋白水平的大幅下降和「斑块排脂」的显著增加。
同时,斑块的逆转的标志,是泡沫细胞和细胞外胆固醇储备的耗尽、巨噬细胞数量的逐渐减少。随着LDL-C从斑块中迁移,抗炎吞噬细胞替代炎症巨噬细胞,后者涉及到清除坏死物质和组织愈合。
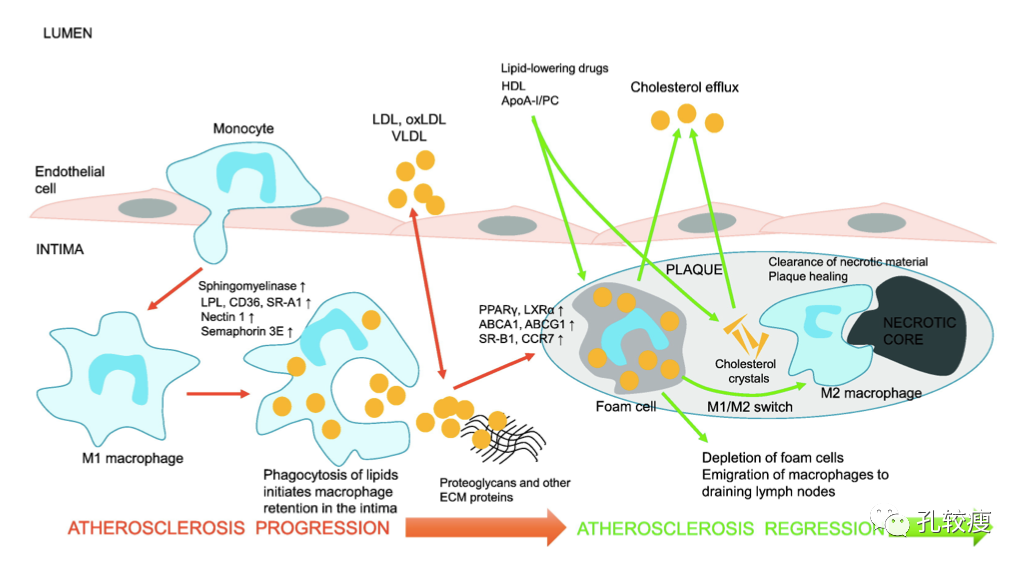
Fig 1. 斑块进展及消退示意图: 通过降低低密度脂蛋白胆固醇和增加高密度脂蛋白胆固醇,可有效改善血浆脂蛋白水平,从而导致斑块消退,其特点是增强胆固醇逆向转运,减少泡沫细胞数量,巨噬细胞迁移,并将残留的巨噬细胞从促炎细胞转变为抗炎细胞,以清除碎片、促进组织修复。巨噬细胞迁移增加与肝X受体和过氧化物酶体增殖物激活受体PPARγ的上调有关。(点击图像可查看大图)
因此,使用降脂药物,如他汀类药物获得良好临床研究的机制,主要是通过减少斑块内巨噬细胞数量,从而诱导易损斑块趋于稳定。巨噬细胞是病变易损性的一个重要标志。这些斑块往往包含脂核较大且富含巨噬细胞。虽然这些斑块仅占整个斑块总数的10-20%,但在急性临床事件中却占80-90%。
二、有关斑块体积变化的IVUS研究
流行病学家和病理学家认识到,在第一次和第二次世界大战期间,营养不良或消瘦患者主动脉或冠状动脉的动脉粥样硬化程度较轻,表明饮食改变可以减少动脉粥样硬化的进展。
从1980年到2000年,人们通过一系列冠脉造影的临床试验,发现血脂水平的下降可以抑制斑块的进展,并引起一定程度的逆转或消退。
IVUS的引入,进一步刺激了动脉粥样硬化进展和消退的观察与研究。这种方法使我们能够定量和定性地观察和测量动脉粥样硬化斑块。
作为一种20世纪90年代发展起来的一种冠状动脉内成像技术,IVUS可用于观察血管壁的细节,并测量血管腔和斑块面积,具有较高的重复性。与冠状动脉造影相比,IVUS提供了更详细的血管壁信息,包括动脉粥样硬化斑块的大小和位置、斑块组织特征和血管重塑。随着IVUS的完善,它基本取代了定量冠状动脉造影,成为动脉粥样硬化进展/逆转试验的主要成像工具。
首项降低LDL-C对冠心病患者斑块消退的影响的IVUS试验,来自日本神户,高木等人发现普伐他汀对动脉粥样硬化的进展有明显的抑制作用,遗憾的的是,他们只研究了靶病变的横截面积,没有分析斑块体积的变化。
2002年,松崎等人对杂合子家族性高胆固醇血症患者,进行了IVUS观察。这项试验中,研究者测量了目标斑块的横截面积。结果提示他汀对动脉粥样硬化斑块有抑制作用,部分患者斑块有轻微消退。
第一次使用IVUS对斑块体积进行分析的试验,是德国的GAIN研究。研究人员用灰阶IVUS测量斑块体积和斑块特征。虽然他们不能识别出斑块的明显消退,但他们确实发现斑块内部回声增强。
REVERSAL研究是一项具有里程碑意义的试验,提示积极降低胆固醇可能带来动脉粥样硬化的逆转。研究者比较了40 mg普伐他汀与80 mg阿托伐他汀对慢性冠心病患者斑块体积的影响,发现普伐他汀组斑块体积进展率较小,但在LDL-C水平为80 mg/dL时,阿托伐他汀组无进展。
ASTEROID试验使用IVUS评估了瑞舒伐他汀他汀对动脉粥样硬化斑块负荷的影响,研究显示当LDL-C处于53 mg/dL时,斑块明显逆转。
ESTABLISH研究,则是在冠状动脉事件发生后半年内通过IVUS连续分析早期、强化的胆固醇管理,对动脉粥样硬化病变的影响。结果显示,阿托伐他汀(20mg)治疗6个月后,LDL-C水平在70 mg/dL下的患者,斑块体积减少13%。斑块体积的百分比变化与LDL-C的降低呈显著正相关,即使在基线水平较低的LDL-C患者中,也是如此。
伴随着这些早期临床试验的发表,医学界相继在CCS和ACS患者中进行了大量的IVUS的临床试验。这些观察一致地发现,积极、强化的脂质修饰可以减少动脉粥样硬化的进展,并导致斑块的消退。
此外,斑块的变化程度与LDL-C水平或LDL-C下降的百分比有关。这些变化在有更多不稳定斑块的ACS患者中更为明显,这些斑块似乎更容易随着LDL-C的降低而倒退。
在PRECISE-IVUS试验中,Tsujita等人证明,他汀联合依折麦布还能进一步减少斑块体积。而且这种趋势,ACS患者比CCS更为显著。
GRAGOV研究是一项评估单用他汀及联合使用PCSK 9抑制剂依洛尤单抗,对斑块逆转作用的大型临床试验。该研究证实,与单用他汀相比,加用pcsk9i后斑块体积变化百分比,自基线减少1%,在基线LDL-C<70mg/dL的亚组中,依洛尤单抗使这一百分比减少更多在。这一研究进一步夯实了降低LDL-C对斑块消退的有效性,并证实了“越低越好”的理论。
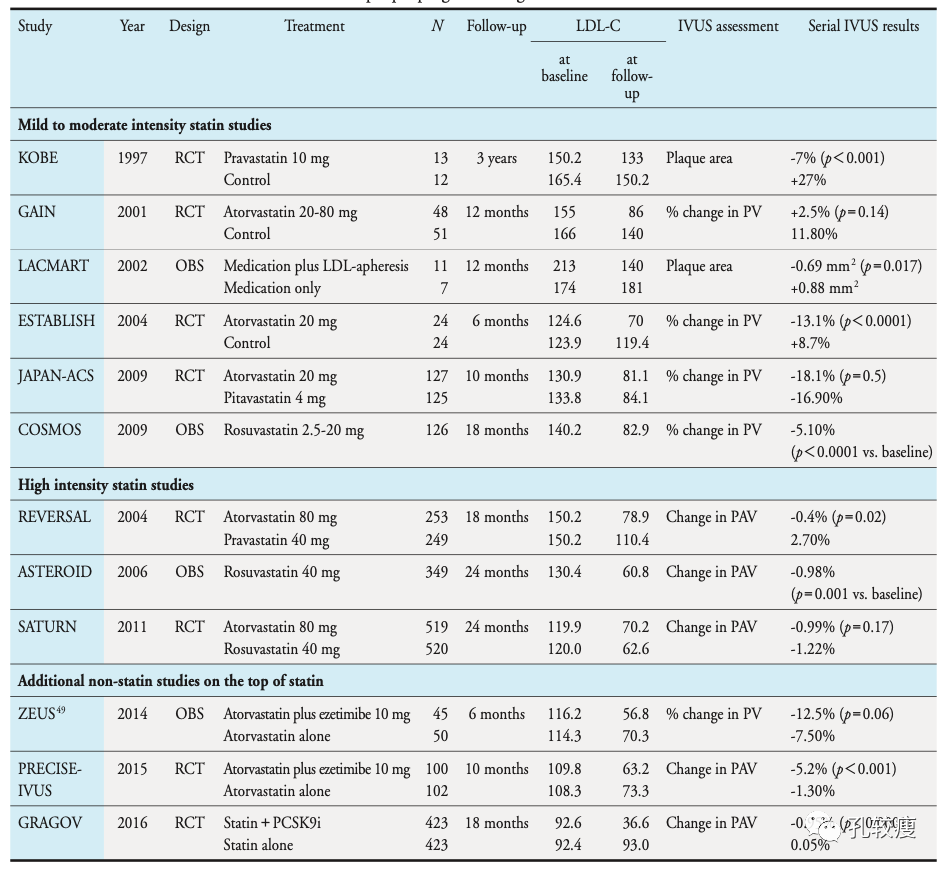
Fig 2. 降胆固醇治疗对斑块体积影响的IVUS研究
(点击图像可查看大图)
三、有关斑块成分变化的IVUS研究
积极降脂治疗,不仅可使得斑块消退,还能稳定不稳定斑块、逆转血管壁正向重构。不稳定斑块的特征是纤维帽薄,脂核大,炎性细胞浸润。

Fig 3. 不稳定与稳定斑块的区别
(点击图像可查看大图)
血管正向重构的血管段常可见此类不稳定斑块。降脂治疗可以使纤维帽变厚,减少脂核,减少炎症细胞浸润:这代表了血管壁正向重构过程的逆转。
如前所述,GAIN研究首次报告了使用灰度IVUS检测斑块特征的变化。进入新世纪后,人们开发了几种IVUS软件来研究斑块特征。Kawasaki等人结果显示,与对照组相比,他汀类药物治疗组斑块的脂类成分显著减少。Nasu等人使用VH-IVUS发现氟伐他汀可以使斑块中纤维-脂肪组织显著减少。Park等人的研究则显示瑞舒伐他汀治疗可改变非罪犯血管的斑块组成和斑块体积。
通过上述系列研究,我们发现,积极降低LDL-C,无论是否减少斑块体积,都可能带来斑块内脂类成分的减少。血管壁的正向重构也因LDL-C的降低而降低。
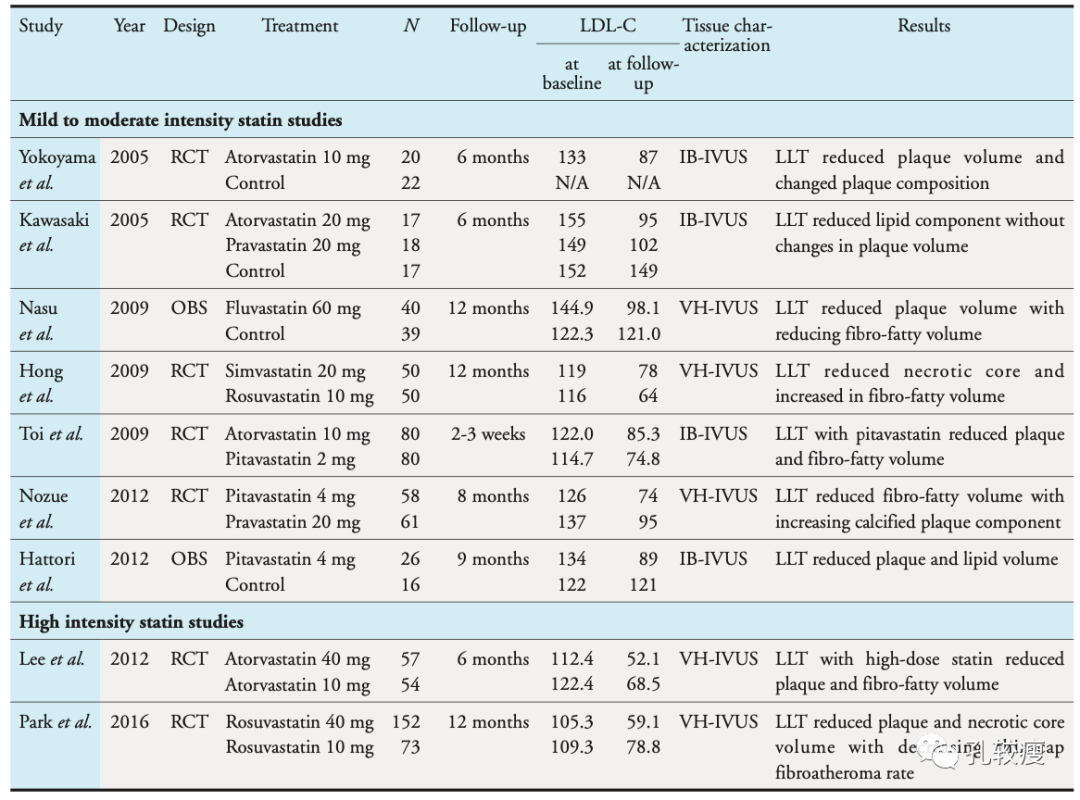
Fig 4. 降胆固醇治疗对斑块成分影响的IVUS研究
(点击图像可查看大图)
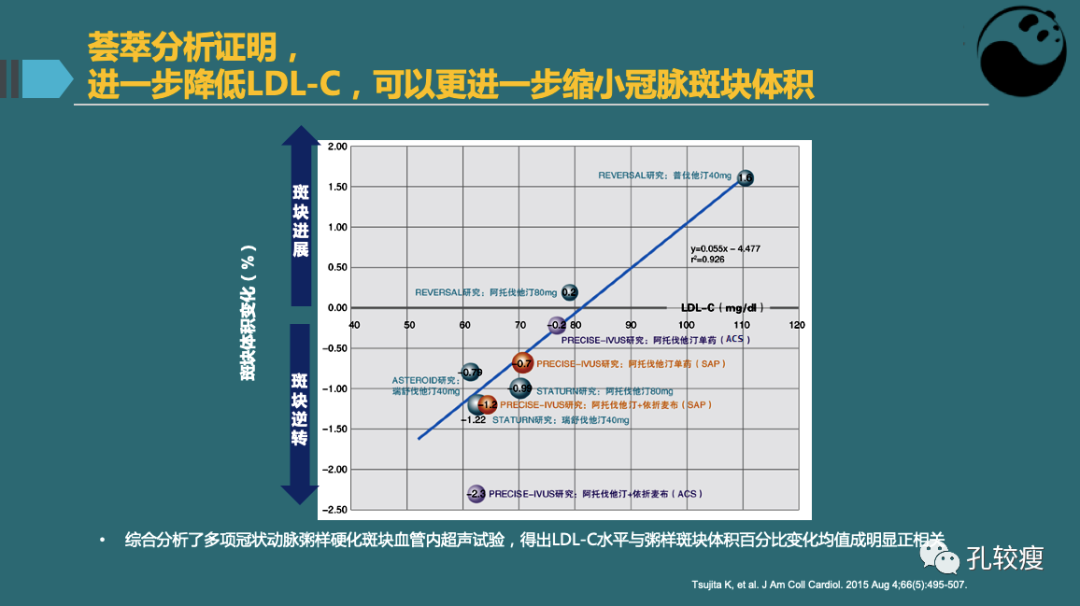 Fig 5. 综合分析了多项冠状动脉粥样硬化斑块血管内超声试验,得出LDL-C水平与粥样斑块体积百分比变化均值成明显正相关(点击图像可查看大图)
Fig 5. 综合分析了多项冠状动脉粥样硬化斑块血管内超声试验,得出LDL-C水平与粥样斑块体积百分比变化均值成明显正相关(点击图像可查看大图)
四、斑块逆转的临床意义
斑块体积的变化是否可以预测未来事件,一直都存在争议。
Nissen等人在IVUS试验中发现,斑块进展患者的事件发生率明显高于斑块消退患者。Dohi等人的研究也发现,在4年的随访后,斑块消退患者的预后明显优于进展者。
但不可否认,IVUS等腔内影像学的应用增加,为预测冠心病患者未来的临床事件,提供了充分而有力的工具。
五、未来发展方向
20世纪初以来,通过降脂使动脉粥样硬化消退一直是一个目标。目前比较确定的共识,是斑块的变化程度与LDL-C的水平或LDL-C降低的百分比有关。
值得注意的是,基于FOURIER等研究结果发表,2019年的ESC血脂管理指南,对ASCVD患者提出了更为激进的目标值(1.4mmol/L)。随着PCSK9抑制剂的使用增多,斑块的逆转及消退有了更为有利的工具。
六、结论
动脉粥样硬化斑块,可以逆转/消退,目前较为肯定的治疗手段是积极降低LDL-C。但由于他汀所能带来的降幅有限,这种趋势并没有想象中的那么理想。随着新型的非他汀类药物的广泛使用,未来我们可能会看到更多的患者出现斑块逆转。
毕竟,当我们有了PCS9抑制剂后,降脂治疗,从来像今时今日一样,那么简单高效。
本文来源:“孔较瘦”微信公众号
孔令秋
复旦大学附属中山医院
成都中医药大学附属医院
心内科 副主任
医学博士
中国CTO老伙计俱乐部成员
中国医药教育协会麻醉超声专委会副主任委员
中国医药教育协会重症超声专委会常委
中国医促会健康医疗与大数据分会委员
中国医促会心血管预防与治疗青年委员会常委
四川省中西医结合学会心血管专委会委员
四川省中医药学会介入心脏病学分会委员
四川省医师协会高血压医师分会青年委员
四川省医师协会心血管内科医师分会青年委员
四川省老年医学会介入专委会委员
四川省老年医学会冠心病专委会委员
中国医疗自媒体联盟成员《BMJ Case Reports》、《中华高血压杂志》《中华心血管病杂志》等期刊审稿人。