引言
心衰新药的问世在一定程度上改善了患者预后,新的药物试验在不断探索,同时针对心衰的器械治疗也再不断进步和更新,器械辅助循环的出现,为终末期心衰的治疗带来一线曙光。器械辅助在抢救心源性休克,长期卸负荷两方面发挥关键作用,并可作为患者等待供体期间的过渡治疗手段。本文将梳理目前心衰治疗领域器械治疗最新进展。
一、主动脉内球囊反搏(IABP)
IABP是一种机械性辅助循环的方法,其基本原理是将球囊导管置于降主动脉内,外接控制装置,随心脏的舒张和收缩进行充气和放气,以增加心输出量,提高冠状动脉的灌注。
适应证:各种原因引起的泵衰竭,如急性梗死并发心源性休克、围手术期发生的心肌梗死、体外循环后低心排综合征、心脏挫伤、病毒性心肌炎、中毒性休克;急性心肌梗死后发生的并发症,如室间隔穿孔、二尖瓣返流、乳头肌断裂、大室壁瘤;内科治疗无效的不稳定性心绞痛;缺血而致的室性心动过速。
禁忌症:主动脉夹层动脉瘤、主动脉瓣返流、出血或不可逆性的脑损害、心脏病、严重凝血机制障碍。
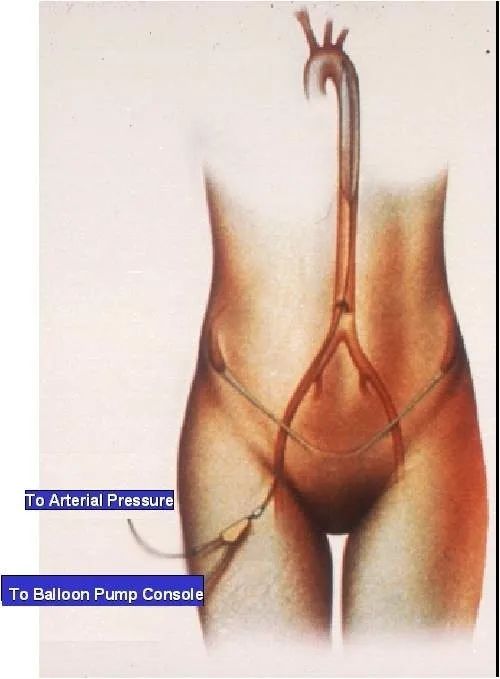
图1 IABP示意图
二、血液净化治疗
适应证:
①出现下列情况之一时:高容量负荷如肺水肿或严重的外周组织水肿,且对利尿剂抵抗;低钠血症(血钠<110mmol/L)且有相应的临床症状如神志障碍、肌张力减退、腱反射减弱或消失、呕吐以及肺水肿等。
②肾功能进行性减退,血肌酐>500μmol/L或符合急性血液透析指征的其他情况可行血液透析治疗。超滤对急性心衰有益,但并非常规手段。
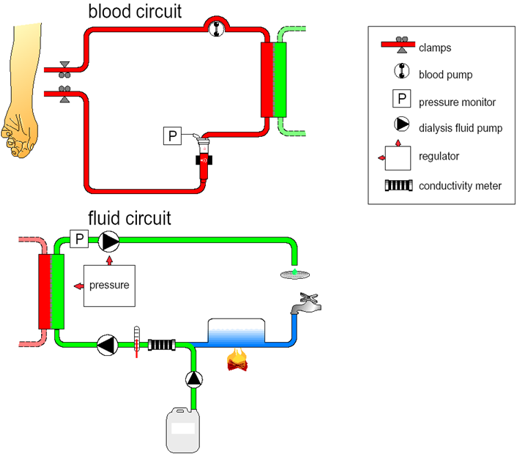
图2 血液净化示意图
UNLOAD研究[1]证实,对于心衰患者,超滤治疗和静脉连续应用利尿剂相比,排水量无明显差异,但超滤治疗能更有效地移除体内过剩的钠,并可降低因心衰再住院率。但CARRESS-HF研究[2]表明,在急性失代偿性心衰合并持续淤血和肾功能恶化的患者中,阶梯式药物治疗方案优于超滤治疗保护,2种治疗患者体重减轻类似,超滤治疗不良反应较高。
三、心脏再同步治疗(CRT)
CRT作为心衰器械治疗的标志性技术,经过近30年的临床研究与实践,已被充分证明能够有效改善患者的心衰症状、运动耐量及生活质量,逆转心肌重塑,并降低心衰住院率和死亡率。
作用机制:CRT采用最佳的房室AV延迟和LV起搏,来增加舒张期充盈时间。室间、室内再同步收缩减少二尖瓣反流,增加每搏输出量。
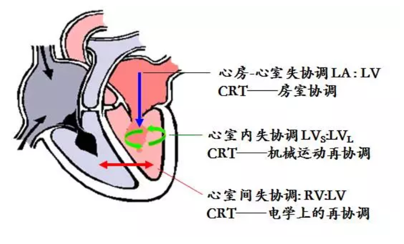
图3 CRT示意图
《中国心力衰竭诊断和管理指南2024》[3]指出,充分的证据表明,心衰患者在药物优化治疗至少3个月后仍存在以下情况应进行CRT,以改善症状及降低病死率。
1. 窦性心律,QRS时限≥150ms,左束支传导阻滞(LBBB),LVEF≤35%的症状性心衰患者(Ⅰ,A);
2. 窦性心律,QRS时限≥150ms,非LBBB,LVEF≤35% 的症状性心衰患者(Ⅱ a,A);
3. 窦性心律,QRS时限120~149ms,LBBB,LVEF≤35%的症状性女性心衰患者(Ⅰ,A)或男性心衰患者(Ⅱa,B);
4. 窦性心律,QRS时限130~<150ms,非LBBB,LVEF≤35% 的症状性心衰患者(Ⅱb,B);
5. 需要高比例(>40%)心室起搏的HFrEF患者(Ⅰ,A);
6. 对于LVEF≤35%的房颤患者,如果心室率难以控制,可于双心室起搏(BIV)后行房室结消融(Ⅱa,B);
7. 已植入起搏器或ICD,LVEF≤35%的HFrEF患者,心功能恶化伴高比例(>40%)右心室起搏,可考虑升级到BIV(Ⅱa,B)。
四、希-浦系统起搏
临床实践中约30%~40%的心衰患者对传统CRT无反应。通过直接起搏希氏束使心脏电活动通过希浦系统传导能够模拟生理性的双心室激动,包括希氏束起搏(HBP)和左束支起搏(LBBP)的新再同步治疗技术正在成为传统CRT的有效补充。
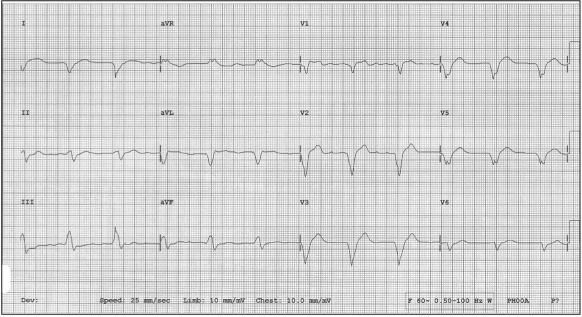
图4 传统起搏方式:将心室电极植入在右心室心尖的肌肉里。与正常人的起搏顺序大相径庭,为非生理性起搏。(心电图类完左)
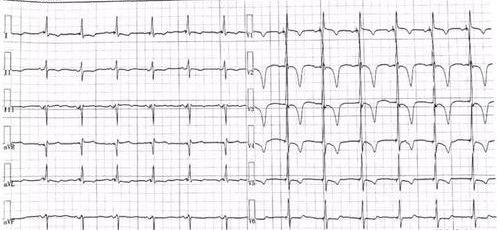
图5 希浦系统起搏:将心室电极直接旋入希浦系统区域,生理性起搏,对心衰患者有利。(心电图波形明显变窄)
《2021 欧洲心脏病学会(ESC)心脏起搏和心脏再同步化治疗指南》[4]指出:
1. 在接受HBP治疗的患者中,建议根据HBP的、特定要求进行设备编程(I类推荐);
2. 对于冠状窦电极植入失败的CRT患者,选择HBP或其他技术(如外科左室心外膜起搏)是合理的(IIa类推荐);
3. 接受HBP治疗的患者,在特定情况下可考虑植入右室电极作为备份起搏电极(IIa类推荐)。
《希氏-浦肯野系统起搏中国专家共识》[5]指出,尽管缺乏足够的临床证据,但无论从理论还是临床实际,在左心室导线植入失败及CRT无反应者中进行补救性希浦系统起搏是合理的。
相较于HBP,LBBP有着相似的临床获益,且操作相对简单、可以越过阻滞部位起搏、起搏阈值低、远期阈值相对稳定,而且在较低输出下即可夺获局部心肌,安全性更高,目前在国内更具应用前景。
五、心脏复律除颤器(ICD)
植入型心脏复律除颤器(ICD)是心衰患者心脏性猝死(SCD)一级和二级预防的重要手段。
各国指南均建议对符合以下标准的患者进行ICD一级预防(I类推荐):
-
2022 ACC/AHA/HFSA心衰管理指南[6]指出,缺血性心衰,纽约心脏协会心功能分级(NYHA分级)Ⅱ~Ⅲ级症状,LVEF≤35%,≥3个月或“慢性”最佳药物治疗,在心肌梗死(MI)后>40天,且预期生存期>1年建议植入ICD。
-
全皮下植入型ICD(S-ICD):晚近的多项研究结果表明,S-ICD与传统TV-ICD具有相似的除颤有效率,并有减少导线相关并发症的趋势。AHA 2022公布的S-ICD PAS研究5年随访的初步结果进一步显示出S-ICD的长期安全性和有效性。
-
血管外植入型ICD(EV-ICD):电极导线植入于胸骨后,较S-ICD更靠近心脏,能够提供心动过缓起搏和三磷酸腺苷(ATP)功能,而且具有体积小、除颤阈值低,使用寿命长(10~12年)等优点。新近发表的EV-ICD Pivotal试验[7]证明了EV-ICD的安全性和有效性,研究发现EV-ICD的除颤成功率达98.7%,围手术期无重大并发症报告,92.6%的患者6个月内无主要的装置或手术相关并发症。
六、左心室辅助装置(LVAD)
左心辅助是将左心房或左心室血流引入辅助泵体,经泵体驱动血流进入主动脉,完全替代左心泵血功能。LVAD效能较IABP高6-8倍,能有效代替心脏80%的工作能力,泵血可达到10L/min。经左心辅助后,左心室室内张力可降低80%,心肌氧需求降低40%,是纠正顽固性心衰和心脏移植前的一种理想治疗手段。
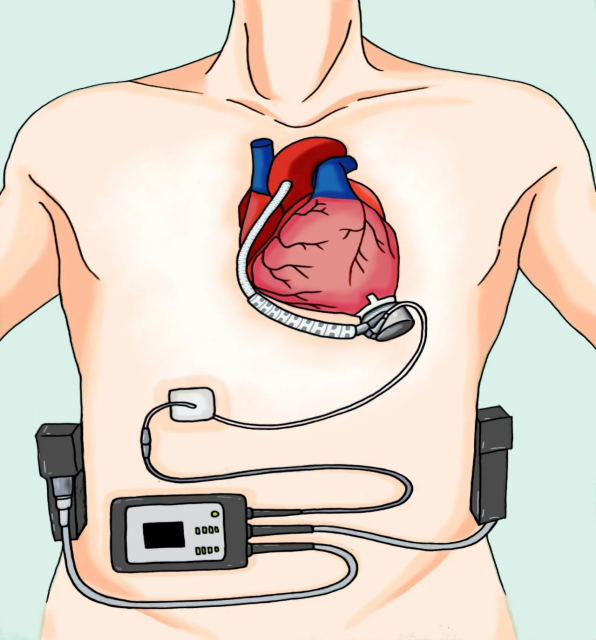
图6 LVAD示意图
适应症:对便用优化的药物和器械淆疗后仍处于终末期心衰的患者,如适合心脏移植,等待心脏移植过程中可置人LAVD或双心室辅助装置(BiVAD) (Ⅰ类,B级)以改善症状,,降低因心衰恶化住院和过早死亡的风险。如不适合心脏移植,,但能以良好的心功能状态预期生存大于1年者,可置人LVAD(Ⅰa类,B级)。
七、植入式心脏收缩力调节器(CCM)
主要针对窄QRS慢性心衰患者。通过微创手术将刺激电极植入到患者心室,在心脏搏动的绝对不应期释放电刺激,这种电刺激不会改变患者心律,但是可以通过一系列信号通路改善心肌的生理状态,能够增强心室肌的收缩力,改善心衰患者心脏功能和临床症状。
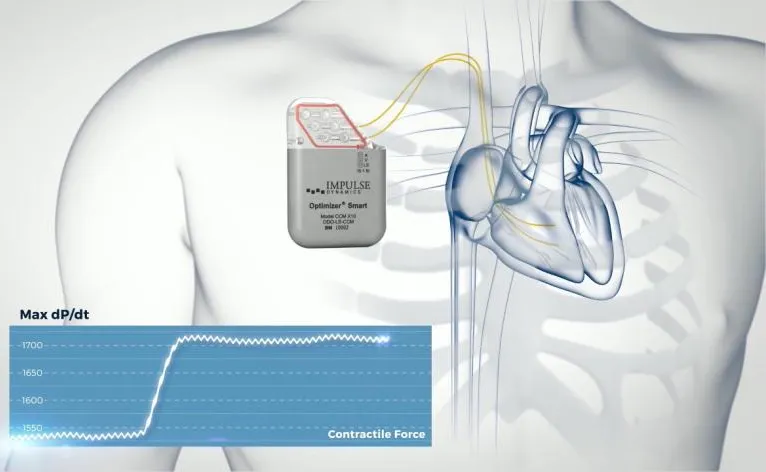
图7 CCM示意图
CCM在不增加心肌负担的情况下,增强心肌收缩力。提高心肌的峰值耗氧量Peak VO2(提高心肌的收缩能力上限)。增加患者的日常活动能力,提高生活质量。降低患者的全因住院率和死亡率。CCM植入操作安全简单,跟普通起搏器植入类似。
适应症:心电图窄QRS<130ms;25%≤LVEF≤45%;药物疗效后仍有症状。
八、心房分流器
心房分流装置是近年来国际上心力衰竭器械治疗的新兴技术,该装置拟通过限定房间隔造口直径,创造稳定可控的左向右分流,有效降低患者左心房压力,缓解肺淤血及呼吸困难症状,同时并不显著增加右心负担、不降低心排量,也不引起反常栓塞。目前研究显示,针对于充分的规范化药物治疗控制不佳的中晚期慢性心衰,房间隔分流器可改善血流动力学障碍引起的肺淤血呼吸困难和反复再住院,改善生存质量和不良预后。目前已有多个产品获得认证上市,如IASD、V-Wave、AFR等。
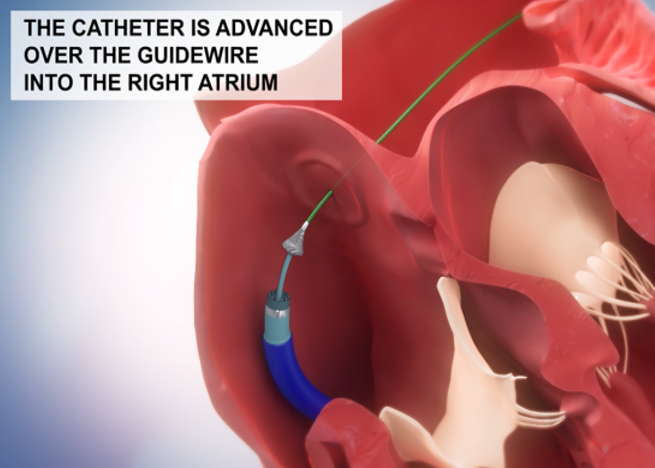
图8 心房分流器
心房分流术仍处于探索阶段,建议对患者适应证进行严格把控。参考国外相关研究及专家共识,建议在以下条件人群中进行心房分流术:(1)经过充分药物治疗仍有症状的左心衰竭患者,过去12个月有因心力衰竭的入院治疗史;(2)BNP或 NT-proBNP升高(窦性心律患者BNP>70pg/ml,房颤患者>200pg/ml,或者窦性心律患者NT-proBNP>200pg/ml,房颤患者>600pg/ml);(3)静息或运动负荷状态下心导管测量PCWP或LAP-右心房压≥5mmHg。同时需排除合并明确的右心功能衰竭的患者,如淤血肝、反复下肢水肿或多浆膜腔积液,或影像学提示右心室直径>左心室、三尖瓣环收缩期运动幅度<12mm、右心室面积变化分数<25%等,或静息状态下右心房压力>14mmHg。
九、其他器械治疗方法
迷走神经刺激疗法(VNS):可对抗交感神经作用,降低肾素血管紧张素-醛固酮系统(RAAS)活性,促进循环NO释放,减少炎症介质。虽然安全性和有效性尚未证实,但开启了慢性心衰神经调节治疗的大门,前景十分广阔。
经导管主动脉瓣置换术(TAVI):针对主动脉瓣狭窄终末期,高龄,一般情况很差,开胸手术换瓣有极大危险的这类严重的主动脉瓣狭窄患者,TAVI展现了更好的结果。近期多项研究显示,TAVI技术可将极高危患者转为低危患者。相信随着器械的进步,手术方法改良,TAVI在心衰治疗方面会成为一个新热点。
经导管二尖瓣缘对缘修复术(TEER):创伤小、恢复快等独特优势,为心衰相关的继发性二尖瓣反流(MR)治疗提供了全新选择。在已进行GDMT但症状持续存在、经食管超声心动图(TEE)显示,二尖瓣解剖结构合适、LVEF 20%~50%、LVESD≤70 mm和PASP≤70 mmHg的患者中TEER具有临床获益(IIa类推荐)。
声明:本文为原创内容,作者小熊,以上仅代表作者本人观点,仅用于学习交流,转载需授权。













