除了已知部分抗肿瘤药物具有潜在的心血管系统毒性外,近来越来越多的研究表明,心血管病和肿瘤两类疾病在流行病学、危险因素以及发生发展机制等方面也存在关联。
近日,Circulation发表的一项研究则显示,动脉粥样硬化是一种平滑肌细胞驱动的肿瘤样疾病,又拉近了肿瘤和心血管病的关系。
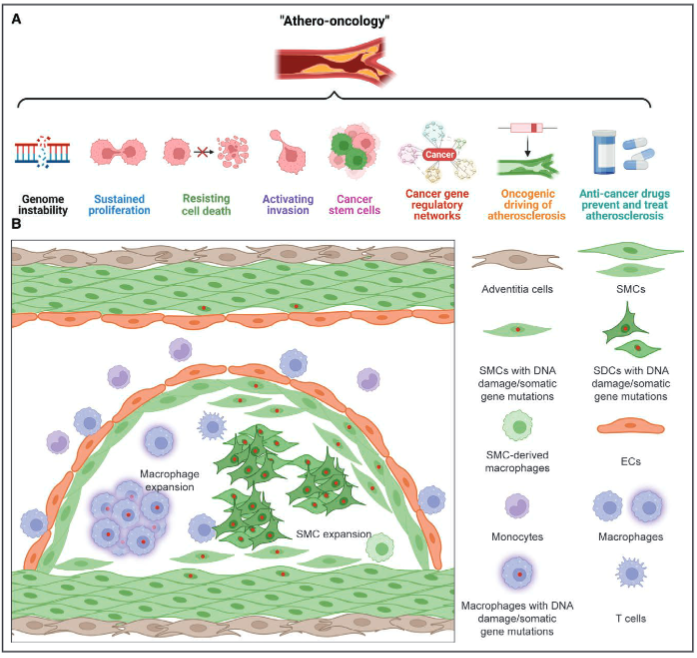
基于当前研究和最近出现的克隆造血动脉粥样硬化机制,作者提出了“动脉粥样硬化肿瘤学”的概念,应认为这是动脉粥样硬化性心血管疾病基础和转化研究的新方向。
动脉粥样硬化涉及多种细胞病理活动,包括免疫细胞(如巨噬细胞和T细胞)、平滑肌细胞和内皮细胞。
越来越多的证据表明,平滑肌细胞向其他细胞类型的转变,即表型转换,在动脉粥样硬化发展和并发症中扮演重要角色。
该研究应用平滑肌细胞谱系追踪小鼠和人体组织,并应用包括分子、细胞、组织学、计算、人类遗传学和药理学方法,分析了平滑肌细胞衍生细胞在动脉粥样硬化中的特征。
结果显示,小鼠和人类动脉粥样硬化中的平滑肌细胞衍生细胞表现出多种肿瘤细胞样特征,包括基因组不稳定、逃避衰老、过度增殖、抵抗细胞死亡、侵袭性和广泛的癌症相关基因调控网络的激活。
致癌突变体KrasG12D的特异性表达加速了平滑肌细胞的表型转换,并加剧动脉粥样硬化。
研究还提供了概念证明:一种靶向DNA损伤修复的抗癌药物尼拉帕尼(niraparib),可以在小鼠模型中减轻动脉粥样硬化进展并诱导晚期疾病病变消退。
研究者表示,这项研究证明,动脉粥样硬化是一种平滑肌细胞驱动的肿瘤样疾病。这一概念促进了对动脉粥样硬化发病机制的理解,也为预防和治疗动脉粥样硬化性心血管疾病进行精准医学策略开辟了前景。
鉴于平滑肌细胞转化与肿瘤的发生多有相似之处,意味着某些化疗方法可能对动脉粥样硬化具有防治作用。
某些抗癌策略,如增强巨噬细胞吞噬(如抗CD47抗体,siRNAs)和抑制细胞增殖(如ATRA)已被证明具有动脉粥样硬化防治作用。而靶向KRASG12C突变而非KRASG12D突变的选择性抑制剂sotorasib,对平滑肌细胞增殖影响很小。
此外,一些抗癌治疗,如免疫检查点抑制剂(例如靶向PD1/PD-L1)可以通过刺激细胞毒性T细胞分泌致动脉粥样硬化细胞因子增加心血管疾病风险。
不同类型抗癌治疗产生的相互矛盾的作用可能反映了动脉粥样硬化中特定细胞类型(如T细胞、巨噬细胞和平滑肌细胞/平滑肌细胞衍生细胞)的不同分子作用,从而影响了临床并发症的风险。
本刊近期一项研究也发现,研究表明,HDL-C <1.23 mmol/L时,动脉粥样硬化性心血管病发生风险增加,而HDL-C较高(≥ 1.84 mmol/L)时,可能增加肿瘤发生风险。
来源:
[1]Pan H, Ho SE, Xue C, et al. Atherosclerosis Is a Smooth Muscle Cell-Driven Tumor-Like Disease. Circulation. 2024 Apr 30.[2]关旭敏, 吴寿岭, 夏云龙, 等. 高密度脂蛋白胆固醇对动脉粥样硬化性心血管疾病及肿瘤发生风险的影响[J]. 中国循环杂志, 2023,38(7): 711-716. DOI: 10.3969/j.issn.1000-3614.2023.07.004.
-END-
声明:本文转载于<中国循环杂志>,仅用于学习交流,版权归原作者所有。如有侵权违规,请立即联系我们。