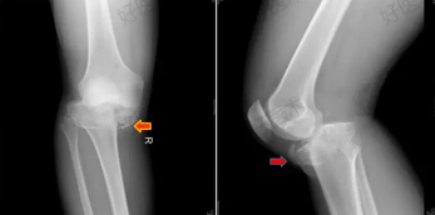
类风湿关节炎(RA)是一种以关节滑膜炎症为主要病理基础、以侵蚀性关节炎症为主要临床表现的慢性、进展性、全身性自身免疫性疾病,可发生于任何年龄段。其病情和病程具有异质性,可出现关节软骨和骨破坏,最终导致关节畸形和功能丧失,还可并发肺部疾病(如间质性肺病)、心血管疾病(RA是发生冠状动脉疾病的独立危险因素)、恶性肿瘤、皮肤疾病(如类风湿结节、皮肤溃疡)、干燥综合征、骨质疏松症、骨折、眼部病变(如巩膜炎、角膜溃疡、虹膜睫状体炎)及抑郁症等。
临床可表现为单关节炎至多关节炎,关节疼痛肿胀,可伴活动受限、晨僵,可能出现乏力、体重下降、低热等全身表现。《类风湿关节炎诊疗规范》(2022年)指出,RA患者预后不佳的危险因素包括关节肿胀数目多、急性期炎症反应物持续高水平、类风湿因子(RF)/抗抗环瓜氨酸多肽(CCP)抗体阳性且呈高滴度、早期出现骨破坏、传统合成改善病情抗风湿药物(csDMARDs)治疗未达标(尤其是2种或多种csDMARDs联合治疗,RA仍处于持续中/高疾病活动度)等。
RA治疗主要依赖药物治疗,目前临床上主要采用早期治疗和达标治疗的治疗策略以改善关节肿痛的症状、控制疾病进展、降低致残率及改善生活质量。《类风湿关节炎诊疗规范》(2022年)中指出,目前RA治疗的首要目标是临床缓解,长病程患者可选择将低疾病活动度作为替代治疗目标。初治或中高疾病活动度的RA患者应每月监测疾病活动度,治疗后达到临床缓解或低疾病活动度的患者,可每3~6个月监测1次;若治疗3个月后疾病活动度改善<50%或6个月未达标者,应及时调整治疗方案。
目前RA治疗药物主要有非甾体类抗炎药物(NSAIDs)、改善病情的抗风湿药物(DMARDs)、糖皮质激素、植物药物等。DMARDs是临床常用且重要的治疗药物,那么,其在RA患者中该如何阶梯化使用呢?
DMARDs发挥作用较慢,故又称“慢作用药物”,其发挥作用大约需1~3个月或6个月,但其可有效控制或延缓疾病的发展。DMARDs包括甲氨喋呤(MTX)、来氟米特(LEF)、柳氮磺吡啶、羟氯喹等csDMARDs以及生物类DMARDs(bDMARDs)和JAK抑制剂(如托法替布、巴瑞替尼)等靶向合成DMARDs(tsDMARDs)。bDMARDs是临床使用最广泛的药物,包括肿瘤坏死因子α(TNF-α)抑制剂(如依那西普、阿达木单抗、英夫利西单抗、赛妥珠单抗、戈利木单抗)、白介素(IL)-6受体拮抗剂(如托珠单抗)、细胞共刺激信号调节剂(如阿巴西普)、抗CD20单抗(如利妥昔单抗)及生物类似药DMARDs。
★ 常用的csDMARDs ★
|
《类风湿关节炎诊疗规范》(2022年)中推荐 |
|||
|
分类 |
药物 |
常规用法用量 |
注意事项 |
|
csDMARDs |
MTX |
1~2个月起效,推荐10~20mg,1次/周,可口服、皮下注射、静脉注射 |
可引起胃肠道反应、骨髓抑制、肝功能异常,围手术期可使用 |
|
LEF |
1~2个月起效,推荐10~20mg,1次/日,可口服 |
可致肝毒性、骨髓抑制,术前及术后均停用一周 |
|
|
柳氮磺吡啶 |
1~2个月起效,推荐1000mg,2~4次/日,可口服 |
可引起皮疹、胃肠不适,围手术期可使用 |
|
|
羟氯喹 |
2~3个月起效,推荐200mg,2次/日,可口服 |
可致眼毒性、皮疹、心脏毒性,围手术期可使用 |
|
★ 常用的bDMARDs和tsDMARDs ★
|
《类风湿关节炎诊疗规范》(2022年)中推荐 |
||||
|
分类 |
药物 |
使用 |
推荐选用及注意事项 |
|
|
生物制剂DMARDs
|
TNF-α抑制剂
|
依那西普 |
可溶性TNF受体-IgG1Fc段融合蛋白,推荐50mg,1次/周,可皮下注射 |
围手术期:术前停用3~5半衰期,术后伤口愈合后再考虑继续使用; ①可阻断RA的炎症级联反应,有快速抗炎、降低RA疾病活动度、阻止骨质破坏的作用。 ②警惕乙型肝炎病毒复制及结核的风险。充血性心力衰竭者避免使用。 |
|
英夫利西单抗 |
人鼠嵌合型TNF-α单克隆抗体,推荐3~10mg/(kg·次),第0、2、6周使用,然后每8周一次,可静脉滴注 |
|||
|
阿达木单抗 |
人源化TNF-α单克隆抗体,推荐40mg,每2周一次,可皮下注射 |
|||
|
戈利木单抗 |
全人源化TNF-α单克隆抗体,推荐50mg,每月一次,可皮下注射 |
|||
|
赛妥珠单抗 |
聚乙二醇化人源化TNF-α单克隆抗体Fab片段,推荐400mg/次,第0、2、4周使用,然后每4周一次,可皮下注射
|
|||
|
IL-6受体拮抗剂 |
托珠单抗 |
托珠单抗是人源化抗IL-6受体的单克隆抗体,常用剂量为8mg/kg,每4周静脉滴注1次 |
①通过与IL-6受体特异性结合抑制IL-6(RA发病的核心炎性介质)介导的炎症级联反应,用于csDMARDs或TNF-α抑制剂治疗效果不佳的活动性RA,可与csDMARDs联用,也可单用。
②不良反应包括感染、血脂异常等。 |
|
|
细胞共刺激信号调节剂 |
阿巴西普 |
阿巴西普是由细胞毒性T淋巴细胞相关蛋白4(CTLA-4)胞外结构域与人IgG1的Fc段组成的融合蛋白,常用剂量为125mg/周,皮下注射
|
①通过阻断T细胞活化所需第二信号抑制T细胞活化,用于治疗对csDMARDs或TNF-α抑制剂疗效不佳的活动性RA患者。 ②严重感染风险可能少于其他生物DMARDs,但有轻微增加肿瘤发生的风险。 |
|
|
抗CD20单抗 |
利妥昔单抗 |
利妥昔单抗是针对CD20的人鼠嵌合单克隆抗体,推荐剂量为每次1000mg,第1天和第15天各静脉滴注1次 |
①通过清除B细胞,抑制自身免疫炎症,主要用于csDMARDs或TNF-α抑制剂疗效不佳的活动性RA患者。 ②用药前需使用糖皮质激素如甲泼尼龙、抗组胺药物预防过敏反应。注意感染的风险,不建议用于合并低丙种球蛋白血症的RA患者。 |
|
|
靶向DMARDs
|
JAK抑制剂 |
托法替布 |
托法替布为JAK1、JAK3的抑制剂,常用剂量为每次5mg,每日2次 |
①JAK是一种非受体酪氨酸蛋白激酶,可介导多种促炎细胞因子胞内信号传导。与生物制剂抑制单个炎性因子不同,JAK抑制剂可同时抑制JAK通路的多种炎性因子,用于对csDMARDs或生物制剂疗效不佳的RA患者。 ②JAK抑制剂导致肿瘤与感染的发生率与TNF-α抑制剂相当;但托法替布可能会增加带状疱疹发生率。 |
|
巴瑞替尼 |
巴瑞替尼为JAK1、JAK2的抑制剂,每次2~4 mg,每日1次 |
|||
《2019年欧洲抗风湿联盟更新了合成类和生物类改善病情抗风湿药在类风湿关节炎中的应用推荐》(2020年)中指出,RA患者一旦确诊应立刻开始DMARDs治疗。若一线csDMARDs治疗未能达标,在不存在预后不良因素的前提下,可考虑使用其他csDMARDs;若存在预后不良因素时,应加用一种bDMARDs或tsDMARDs治疗,bDMARDs和tsDMARDs应和一种csDMARDs联用。
RA患者应尽早开始使用DMARDs治疗,以预防或减慢关节的进一步破坏。csDMARDs可影响异常免疫功能,延缓或控制病情进展、保护关节功能的完整性、减少或防止关节破坏,但无明显的镇痛和抗炎作用。其目前仍是RA治疗的一线用药,其中MTX作为基石药物,推荐单药治疗,存在MTX禁忌或不耐受时,可考虑LEF或柳氮磺吡啶。
《2015年亚洲太平洋地区风湿病学学会联盟类风湿关节炎治疗建议》中指出,csDMARDs治疗不充分或不耐受时,可选用生物制剂DMARDs。tsDMARDs可用于对MTX治疗应答不充分或不耐受的中重度活动性RA患者。
csDMARDs起效较慢,故在中、高疾病活动度RA患者中可联合糖皮质激素作为桥接治疗,以快速控制症状。糖皮质激素具有高效抗炎与免疫抑制作用,还可镇痛,迅速减轻关节肿胀,可缓解多数RA患者的症状,并作为DMARDs起效前的“桥梁”作用,但其不能阻止RA病程进展与关节破坏,不建议长期使用,可在3个月内逐渐减停。
《类风湿关节炎诊疗规范》(2022年)中指出RA患者治疗达标后药物减停的原则,即病情得到控制的RA患者应在3个月内停用糖皮质激素,停药后在继续维持csDMARDs治疗的前提下,已经维持达标状态至少6个月者可逐渐减停靶向药物,停药后仍处于持续临床缓解者,可考虑减量csDMARDs,但需严密监测病情,谨防复发。因RA是一种慢性疾病,不建议停用csDMARDs。
csDMARDs治疗3个月疾病活动度改善<50%或6个月未达标者,可根据有无合并预后不良因素调治疗方案。
《2018中国类风湿关节炎诊疗指南》指出,单一csDMARDs治疗未达标时,建议联合另1种或2种csDMARDs进行治疗;或一种csDMARDs联合一种生物制剂DMARDs进行治疗;或一种csDMARDs联合一种靶向合成DMARDs进行治疗。
对无预后不良因素者,可在原有单药治疗的基础上,联合另1种或2种csDMARDs治疗继续观察,如MTX联合LEF、MTX联合柳氮磺吡啶、MTX联合羟氯喹、MTX联合柳氮磺吡啶及羟氯喹等。
对合并预后不良因素或糖皮质激素减停失败者,可联用一种靶向药物(生物原研DMARDs或生物类似药DMARDs或靶向合成DMARDs)治疗,靶向药物可抑制RA的核心致炎因子或关键免疫细胞的功能,快速缓解RA病情,其选择无优先推荐。
《欧洲抗风湿病联盟关于改善病情的抗风湿药物治疗类风湿关节炎的15项建议》中指出,初始csDMARDs治疗失败后,如存在预后不良因素可考虑加用生物制剂DMARDs。《2018中国类风湿关节炎诊疗指南》中指出,目前TNF-α抑制剂、托珠单抗和托法替布在使用的选择上并无优先顺序。当csDMARDs联合其中一种治疗未达标后,可在三者间更换另外一种进行治疗。《2015年亚洲太平洋地区风湿病学学会联盟类风湿关节炎治疗建议》中指出,若存在不良预后因素且处于疾病活动期,考虑尽早使用生物制剂DMARDs。
潜伏结核感染者行预防性抗结核治疗至少1个月后方可开始靶向治疗,然后每3个月进行结核评估;活动性结核感染者至少完成3~6个月的抗结核治疗,且痰抗酸杆菌检测为阴性后方可采用靶向治疗,抗结核治疗需持续9~12个月。
一种生物DMARDs或靶向合成DMARDs治疗RA未达标时,可考虑换用另一种靶向药物,优先考虑换用另一种作用机制的生物DMARDs或靶向合成DMARDs。
对TNF-α抑制剂治疗失败的RA患者,可考虑换用另一种TNF-α抑制剂继续治疗,与传统抗风湿药物相比,其起效快、延缓或抑制骨破坏的效能明显。
生物制剂DMARDs有良好的抗炎和阻止疾病进展的作用,tsDMARDs可减轻免疫反应造成的组织损伤。二者都可缓解RA患者的临床症状、躯体功能障碍,阻止影像学进展。
- 参考文献 -
声明:本文来源风湿免疫界,仅为交流学习。内容仅代表作者个人观点,望大家理性判断及应用。