不少心绞痛和心肌梗死的患者冠脉造影并未见显著的狭窄,也有很多患者行经皮冠状动脉介入治疗(PCI)术后尽管支架通畅,但是仍有胸闷、心绞痛等症状。这一现象困惑着心血管医师数十年,直到近20年,随着循证医学和介入及影像技术等的快速发展,人们才逐渐认识到冠状动脉微血管疾病也是造成心肌缺血的重要原因。
冠状动脉微血管疾病(Coronary microvascular disease, CMVD)是指在多种致病因素的作用下,冠状前小动脉和小动脉的结构和(或)功能异常所致的劳力性心绞痛或心肌缺血客观证据的临床综合征。以前也叫做X综合征、微血管性心绞痛、微血管功能异常等名称。冠状动脉包括心外膜下冠状动脉(直径>400μm)、前小动脉(直径<400μm)、小动脉(直径<100μm)、毛细血管(直径<10μm),其中心外膜下冠脉主要负责血流传输,前小动脉和小动脉即属于冠脉微血管,前小动脉在心外膜冠状动脉灌注压或血流量发生改变时,通过血管舒缩稳定小动脉的压力,近端对压力敏感,远端对流量敏感。小动脉根据心肌代谢的需求调节血管张力和血流量。毛细血管则主要负责血氧交换。前小动脉与小动脉可以自动感知压力、流量、心肌代谢废物等,并自动调整心肌灌注,故冠脉微循环障碍时,也可出现严重的心肌缺血。
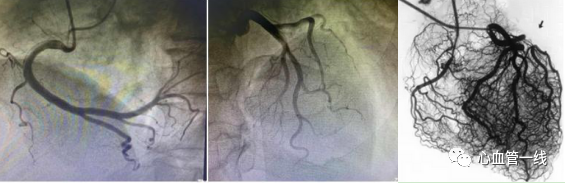
冠脉造影只能看到直径>400-500μm的大血管,而冠状动脉微血管占整个冠脉树的90%以上,却无法被冠脉造影显示。若仅以冠脉造影能看见的心外膜下冠脉的异常来诊断评估“冠心病”,显然是“只见树木,不见森林”。
图1 冠脉造影看到的右冠(左)、左冠(中)和真正的冠脉循环(右)
以往的临床研究显示,在具有心肌缺血症状但冠脉造影显示非阻塞性病变(冠脉狭窄<20%)的患者中,CMVD的发生率约为45%~60%,2012年欧洲学者对稳定型心绞痛患者进行7.5年的长期随访,结果显示冠脉造影正常和非阻塞性冠状动脉病变患者的主要心血管事件和全因死亡率显著高于对照人群,CMVD很可能是导致这些患者不良预后的重要原因。故CMVD的检出和治疗具有十分重要的意义。
CMVD涉及的患者人群广泛,常见于非阻塞性冠心病、肥厚型心肌病、高血压病、糖尿病、肥胖、吸烟、女性冠心病患者、PCI术后患者和心梗后患者等。肥厚型心肌病和高血压病患者室壁间小动脉内中膜增厚、管腔变窄导致微血管结构异常,而糖尿病、肥胖、吸烟以及合并其他心血管疾病危险因素的患者往往存在冠脉微血管功能异常,其机制包括内皮细胞依赖性血管舒张异常、内皮细胞非依赖性血管舒张异常、微血管缩窄、微血管栓塞、以及血管外机制,血管外机制常见于左室舒张压明显升高的疾病如左心室肥厚、左心室纤维化等,以及可直接降低冠状动脉舒张压的疾病如主动脉瓣狭窄、前小动脉缩窄、低血压等。因此,CMVD与微血管性心绞痛、心肌梗死、缺血再灌注损伤、冠脉无复流、慢血流等现象密切相关,对这些CMVD高危患者需要积极关注冠脉微血管病变,及早干预、不容忽视。
大约30%~60%的CMVD患者有心绞痛症状,可表现为劳力性心绞痛发作、休息后缓解。休息时发作的非典型心绞痛也很常见。还可表现为不稳定型心绞痛,运动耐量逐渐降低或运动时呼吸困难,伴心衰的CMVD患者可能存在典型的静脉充盈压升高的表现,例如颈静脉压增高、肺部啰音和下肢水肿等。
2019年ESC慢性冠脉综合征指南将稳定性冠心病更名为慢性冠脉综合征,建议当患者存在明确的心绞痛症状、无明显心外膜冠脉阻塞性狭窄且非侵入性检查(如负荷心电图、经胸多普勒超声心动图、磁共振和放射性核素心肌灌注显像)结果异常时,应怀疑非阻塞性原因,如冠脉痉挛和CMVD所致心肌缺血。
目前冠状动脉微血管功能常通过检测冠状动脉微血管对血管扩张剂的反应来评价,测量指标是应用血管扩张剂后冠状动脉微血管呈最大限度扩张时的冠状动脉血流量与基础状态下冠状动脉血流量的比值(冠脉血流储备,CFR),CFR<2.5提示冠状动脉微血管舒张功能异常,临床上以CFR<2.0作为诊断微血管功能障碍的界值。常用的血管扩张剂包括腺苷、双嘧达莫、乙酰胆碱,前两者为内皮非依赖性,后者为内皮依赖性,需冠脉内注射。
正电子发射型断层显像(PET)心肌血流定量是无创测定CFR的金标准。其他多种无创影像技术也可用于CMVD的检测诊断,如心脏磁共振负荷/静息心肌灌注成像、经胸多普勒超声心动图(TTDE)负荷/静息测量冠脉血流速度、单光子发射计算机断层成像技术(SPECT)等。有创的评价手段包括选择性冠脉造影观察冠脉显影速度和心肌显影速度、冠状动脉内多普勒血流导丝技术测量冠脉血流速度计算CFR和冠脉微血管阻力(CMR)、以及温度稀释法测算CFR等。
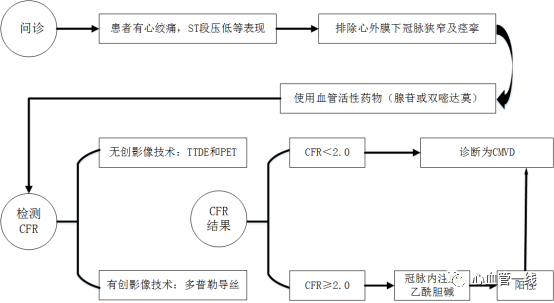
根据冠状动脉微血管疾病诊断和治疗的中国专家共识,诊断CMVD的步骤为:
(1)临床疑诊CMVD的患者,在排除心外膜下冠状动脉狭窄和痉挛病变后,应首先采用静脉注射腺苷或双嘧达莫的方法并选用TTDE、CMR 或PET等无创性影像技术测量CFR。
(2)在上述患者中,如无创性技术测量的CFR≥2.0,可在冠状动脉注射腺苷前后,采用冠状动脉内多普勒血流导丝技术测量CFR和CMR。如冠状动脉内多普勒血流测量的CFR≥2.0,应选择冠脉内注射乙酰胆碱的方法,心外膜下冠脉无痉挛但出现心绞痛症状和缺血型ST-T改变,可诊断为 CMVD,同时应立即冠脉内注射硝酸甘油或尼可地尔对抗冠脉微血管痉挛。
CMVD分为不合并阻塞性冠状动脉疾病的CMVD、合并阻塞性冠状动脉疾病的CMVD、其它类型的CMVD三类。其中不合并阻塞性冠状动脉疾病的CMVD又包括原发性稳定型微血管心绞痛和原发性不稳定型微血管心绞痛。
② 静息或负荷状态下心肌缺血的客观证据(ST段压低、心肌灌注缺损或心肌代谢产物增多)但无节段性室壁运动异常
④ 冠脉造影或冠脉CTA检查无明显心外膜下冠脉狭窄(冠脉狭窄<20%)
① 患者有典型不稳定型心绞痛或急性非ST段抬高型心肌梗死但硝酸甘油疗效不佳
② 心电图缺血型ST-T改变并呈动态演变,血清肌钙蛋白水平可有轻度升高
如具备其它条件但CFR≥2.0,可行冠状动脉内注射乙酰胆碱的激发试验。如心外膜下冠状动脉无痉挛但出现心绞痛症状和心电图缺血型ST-T改变亦可确诊。
合并阻塞性冠状动脉疾病的CMVD包括稳定型心绞痛、急性冠脉综合征和急诊PCI后CMVD。在阻塞性冠状动脉病变所导致的稳定型心绞痛患者,如心绞痛发作时间较长、发作程度重于冠脉狭窄程度所预期的症状、诱发心绞痛的体力活动阈值变异大且硝酸甘油无效,应考虑到合并CMVD的可能。在PCI治疗解除心外膜冠状动脉狭窄病变后,如注射腺苷或双嘧达莫后测量的CFR<2.0或冠脉内注射乙酰胆碱后心外膜下冠状动脉无痉挛但出现典型心绞痛和心电图缺血型ST-T改变,可诊断合并CMVD。此外,在接受直接或择期PCI后的患者,如血流分级<3级和(或)心肌血流灌注分级(TMPG)<3级,应考虑CMVD。PCI后出院前SPECT 显像显示心肌局部无灌注区或CMR显示心肌灌注缺损或钆延迟显像增强,可诊断CMVD。
其他类型的CMVD包括应激性心肌病、肥厚型心肌病、扩张型心肌病、心肌炎、主动脉瓣狭窄、Anderson-Fabry 病、心肌淀粉样变性等,这些疾病的发病机制中可能有CMVD的参与,但尚无特异性的治疗办法。
1.控制危险因素 包括戒烟、减轻体重、充分控制血压、治疗糖尿病和相关的代谢异常、良好的血脂管理、合理膳食和定期运动等。高血压患者首选血管紧张素转化酶抑制剂(ACEI)和血管紧张素受体拮抗剂(ARB)治疗。他汀类可改善动脉粥样硬化和内皮功能。
2.抗缺血治疗 尼可地尔是治疗原发性稳定型微血管心绞痛的首选推荐药物。一线抗缺血药物还有β受体阻滞剂或非二氢吡啶类钙拮抗剂,若效果欠佳可联合应用上述两种药物,若不能耐受β受体阻滞剂可采用伊伐布雷定代替。也可采用雷诺嗪、ACEI控制心绞痛症状。对原发性不稳定型微血管心绞痛,可选用咪贝拉地尔和法舒地尔治疗,后者对微血管痉挛有效。
3. 防治微血管阻塞 对接受直接PCI治疗的急性ST段抬高型心肌梗死的患者,如冠脉血栓负荷较重可使用血栓抽吸术,此外,多项研究表明术前或术中应用血小板糖蛋白IIb/IIIa受体拮抗剂、腺苷、尼可地尔、维拉帕米、地尔硫卓、硝普钠、山莨菪碱、前列地尔、曲美他嗪、通心络等药物可降低无复流、慢血流等的发生率。
冠状动脉微血管疾病在人群中患病率高,大大增加了患者远期心血管事件的风险,但目前仍存在着临床重视不足、发病机制不清、临床表型复杂、诊断技术有限、长期疗效不详等问题。为改善CMVD远期预后,临床医师及时识别并给予适当的治疗是非常重要的。
郑州大学一附院心血管病医院心内科 梁翠
主审 张彦周
声明:来源心血管一线。仅用于学习交流,版权归原作者所有,如涉及图文、版权或其它问题,请及时与我们联系,我们将立即删除。文内观点仅代表作者个人,望大家理性判断及应用!